Свойство - реагирующая молекула
Cтраница 1
Свойства реагирующих молекул, например их массы, входят в знаменатель множителя Fj JF & FB, тогда как подобные величины в выражении для числа столкновений Z входят в числитель. Поэтому с первого взгляда может показаться, что результаты теории столкновений и статистической теории должны быть несовместимы. Однако следует напомнить, что активированный комплекс получается из реагирующих веществ и, следовательно, величины, характеризующие свойства последних, содержатся также и в числителе дроби Г JF F Тем не менее, как и следовало ожидать, оба метода не обязательно приводят к одинаковым результатам. [1]
Если известна энергия активации, то можно рассчитать константу скорости элементарной реакции через свойства реагирующих молекул и активированного комплекса. [2]
Большой принципиальный интерес представляет, однако, возможность расчета абсолютных скоростей реакций исходя непосредственно из свойств реагирующих молекул. Раздел химической кинетики, занимающийся этим вопросом, носит название теории абсолютных скоростей реакции. [3]
Большой принципиальный интерес представляет, однако, возможность расчета абсолютных скоростей реакций, исходя непосредственно из свойств реагирующих молекул. [4]
Таким образом, константа скорости мономолекулярных реакций согласно теории РРКМ при низких давлениях зависит только от свойств реагирующих молекул и высоты энергетического барьера и не зависит от свойств активированного комплекса. [5]
Надо иметь в виду, что теория активных соударений не дает возможности теоретического расчета энергий активации исходя из свойств реагирующих молекул. Она только обосновывает даваемую уравнением Аррени-уса зависимость константы скорости от температуры. [6]
Надо иметь в виду, что теория активных соударений не дает возможности теоретического расчета энергий активации исходя из свойств реагирующих молекул. Она только обосновывает даваемую уравнением Аррениуса зависимость константы скорости от температуры. При всех расчетах по TAG величина Е находится из эксперимента. [7]
Как указывалось выше, константа равновесия для образования активированного комплекса, К, может быть вычислена по данным о свойствах реагирующих молекул и о предполагаемых свойствах комплекса. Это означает, что константу скорости k ( или k2) можно вычислить из первых принципов, подобно тому как это может быть сделано в теории столкновений. В табл. 22 - 2 сопоставляются вычисленные в рамках этих теорий константы скорости нескольких реакций с экспериментальными данными. [8]
 |
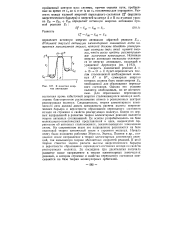
К понятию энергии активации. [9] |
Следовательно, теория элементарного химического акта должна давать возможность расчета высоты энергетического барьера и вероятности образования переходного состояния исходя из строения и свойств реагирующих молекул. Одним из первых направлений в развитии теории элементарных реакций является теория активных столкновений. [10]
 |
К понятию энергии активации. [11] |
Следовательно, теория элементарного химического акта должна давать возможность расчета высоты энергетического барьера и вероятности образования переходного состояния исходя из строения и свойств реагирующих молекул. Одним из первых направлений в развитии теории элементарных реакций является теория активных столкновений. [12]
Вещества, обладающие такой двойственной функцией, при смешении их с реагирующей системой, в зависимости от условий, проявляют себя в одних случаях как замедлители, а в других - как ускорители. Это различное действие примесей зависит как от свойств реагирующей молекулы, так и от температуры. [13]
Оптической плотностью называется десятичный логарифм отношения интенсивности падающего света к интенсивности света, прошедшего через раствор. Теория абсолютных скоростей химических реакций позволяет рассчитать константу скорости на основании данных о свойствах реагирующих молекул и об условиях протекания реакции. Число сталкивающихся и число вступающих в реакцию молекул всегда различаются, так как к реакции способны не все сталкивающиеся молекулы, а только активные, кроме того, даже активные молекулы при столкновении могут не вступить в реакцию, что учитывается стери-ческим фактором. [14]
Теория таких процессов представляет значительный интерес особенно потому, что многие аспекты теории теперь достигли уровня, позволяющего практически рассчитывать скорость реакций на основании свойств реагирующих молекул. Хотя основы современных теорий были заложены приблизительно сорок лет назад, применение имевшихся теоретических методов к опытным данным оставалось ограниченным. Главной причиной отсутствия прогресса в этом направлении является значительная сложность современных теорий. В этой книге сделана попытка исправить существующее положение путем детального обсуждения вывода основных уравнений и их иллюстрацией численными примерами. [15]
Страницы: 1 2