Свойство - реагирующая молекула
Cтраница 2
Статьи, вошедшие в сборник, отражают современное состояние исследований нуклеофильного и электрофильного замещения при насыщенном углеродном атоме и в ароматическом ряду. Большое внимание уделено переходному состоянию, роли и строению промежуточных частиц, в том числе классических и неклассических ионов и ион-радикалов, влиянию среды, свойств реагирующих молекул и продуктов реакции. Описано применение ЯМР -, ЭПР-и фотоэлектронной спектроскопии для исследования кинетики и механизмов реакций. Показаны возможности использования явления химической поляризации ядер для выяснения и изучения актов одноэлектронного переноса. [16]
Как показывает опыт, этот закон строго выполняется для большинства химических реакций. Таким образом, исследуя зависимость скорости индивидуальной реакции от температуры, представляется возможным вычислить величину энергии активации, являющуюся важной кинетической константой, зависящей от химического строения и свойств реагирующих молекул. Для этих целей определяют скорость реакции при нескольких ( 5 - 6) значениях Т и прочих одинаковых условиях. По тангенсу угла наклона определяют величину энергии активации. Разумеется, при расчете энергии активации способ графического выражения данных должен быть учтен. [17]
Для того чтобы произошла химическая реакция, сначала молекулы должны сблизиться до довольно малого расстояния, или, как говорят, молекулы должны столкнуться. Теория, описывающая на основании свойств реагирующих молекул кинетику реакции, тем или иным образом решает как задачу расчета чисел столкновений реагирующих молекул, так и задачу о собственно химическом превращении в комплексе столкнувшихся частиц. [18]
Первая задача связана с решением уравнения Шредингера ( см. § 13.1) для системы частиц, образующих активированный комплекс. Эта проблема очень сложная и решается приближенно с помощью ЭВМ. Поэтому в основном теория развивается в поисках методов оценки энергии и энтропии образования активированного комплекса исходя из свойств реагирующих молекул. [19]
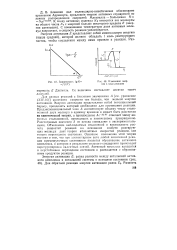 |
Зависимость lg К.| Изменение энергии в ходе реакции. [20] |
Энергия активации представляет собой потенциальный барьер, преодолеть который необходимо для протекания реакции. Предэкспоненциальный член А соответствует общему числу столкновений двух молекул в единицу времени и может быть рассчитан из кинетической теории, а произведение Ae-ElRT отвечает числу активных столкновений, приводящих к химическому превращению. Рассчитанные значения А не всегда совпадают с экспериментальными. Объяснение наблюдаемых отклонений и возможность расчета скоростей реакций на основании свойств реагирующих молекул дает теория абсолютных скоростей реакции, или теория переходного состояния. Основное положение этой теории состоит в том, что при элементарном акте любой химической реакции промежуточным состоянием является образование активного комплекса, в котором в результате сильного соударения происходит перегруппировка валентных связей. Активный комплекс находится в неустойчивом переходном состоянии и распадается с образованием продуктов реакции. [21]
Основное положение теории абсолютных скоростей химических реакций заключается в том, что всякий элементарный химический акт протекает через переходное состояние ( активированный комплекс), когда в реагирующей системе исчезают отдельные связи в исходных молекулах и возникают новые связи, характерные для продуктов реакции. Первая задача связана с решением уравнения Шредингера для системы частиц, образующих активированный комплекс. Эта проблема очень сложна и в настоящее время приближенно решается с помощью современных ЭВМ только для простейших реакций. Поэтому в основном теория развивается в поисках методов оценки энергии и энтропии образования активированного комплекса исходя из свойств реагирующих молекул. [22]
При переходе от углеводородов к молекулам, содержащим гетеро-атомы, помимо указанных выше неучитываемых факторов, появляются новые осложнения, в конечном счете связанные с различной электроотрицательностью атомов углерода и гетероатомов. Электронные смещения в реагирующих молекулах и радикалах, вызванные различной электроотрицательностью атомов, могут в различной степени влиять на уровень начального и переходного состояний. Особенно сильное влияние на переходное состояние можно ожидать в том случае, когда реагирующие частицы включают группы, обладающие различными донорно-акцептор-ными свойствами по отношению к электронам. Можно ожидать, что в этом случае энергия сопряжения в переходном состоянии окажется больше, чем в начальном и конечном состояниях, когда акцепторная и донорная группы не находятся в сопряжении. В этом случае условие монотонного изменения общей энергии сопряжения системы в ходе реакционного акта не соблюдается, уравнение ( 12) перестает быть справедливым и изложенная выше теория не применима. Если акцепторно-донорные свойства реагирующих молекул ( радикалов) не сильно различаются, то, как показывает анализ опытных данных ( см. ниже), теория идеальной радикальной реакционности в общих чертах может быть применена и к молекулам, содержащим гетероатомы. [23]
Следовательно, теория элементарного химического акта должна давать возможность расчета высоты энергетического барьера и вероятности образования переходного состояния исходя из строения и свойств реагирующих молекул. Одним из первых направлений в развитии теории элементарных реакций является теория активных столкновений. На современном этапе это направление развивается на базе квантовой теории химической связи и строения молекул. Начало этому было положено работами Эйринга, Эванса, Поляни и др., создавших новое направление в теории элементарных химических реакций, так называемую теорию абсолютных скоростей реакций. В этой теории ставится задача расчета высоты энергетического барьера и вероятности образования переходного состояния исходя из свойств реагирующих молекул. За последние три десятилетия получило развитие новое направление в теории элементарных химических реакций, в котором строение и свойства переходного состояния описываются на базе теории молекулярных орбиталей. [24]
Это равносильно утверждению, что при достаточно низких давлениях все активные молекулы реагируют; значит, скорость реакции определяется скоростью активации, и скорость образования А из А более не существенна. Выражение для скорости активации можно получить, как и ранее, рассматривая равновесие М А5 МгА; при равновесии скорость активации равна скорости дезактивации &. А в результате реакции ( разд. Статистические множители отсутствуют, поскольку они появляются в константе скорости ka образования А из А, которая не влияет на скорость реакции. Аналогично в формуле (4.23) отсутствует множитель, связанный с адиабатическим вращением; этот недостаток первоначального метода Маркуса исправляется в более поздних вариантах, обсуждаемых в разд. Однако, за исключением этого замечания, получается интересный результат: константа скорости при низких давлениях зависит только от свойств реагирующих молекул и высоты энергетического барьера и не зависит от свойств активированного комплекса. [25]
Страницы: 1 2