Свойство - реальный раствор
Cтраница 1
Свойства реальных растворов отличаются от свойств идеальных, однако в большинстве случаев приближение к идеальной модели оказывается достаточным для того, чтобы было удобно рассматривать отклонения от этой модели. [1]
Свойства реальных растворов нередко существенно отличаются от свойств идеальных систем. При этом термические, энтропийные, объемные и прочие эффекты неидеальности могут наблюдаться в одной и той же системе. [2]
Свойства реальных растворов описываются уравнениями, в которых вместо давления и концентрации вводятся летучесть и активность. [3]
Свойства реальных растворов описываются уравнениями, в которых вместо концентраций вводится активность. [4]
Вычисление свойств реальных растворов в широком диапазоне давлений и температур представляет собой чрезвычайно сложную и иногда практически неразрешимую задачу, что отчасти видно из способа расчета парциальных мольных величин. [5]
Описание свойств реальных растворов требует, помимо термодинамических соотношений, сведений об урав нении состояния. [6]
Вычисление свойств реальных растворов в широком диапазоне давлений и температур представляет собой чрезвычайно сложную и иногда практически неразрешимую задачу, что отчасти видно из способа расчета парциальных мо-лярных величин. [7]
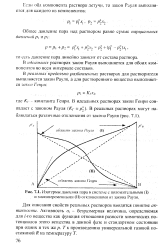 |
Изотермы давления пара в системе е положительными (. и знакопеременными ( II отклонениями от закона Рауля. [8] |
Для описания свойств реальных растворов вводится понятие активности. [9]
Представления, что свойства реального раствора в большой степени обусловлены происходящими в нем реакциями ассоциации, развивались во многих последующих работах. Исследование специфических взаимодействий - важная задача современной физической химии растворов, и решение этой задачи опирается на достижения экспериментальных физических методов исследования ( прежде всего, спектральных), теории межмолекулярных взаимодействий и теории растворов. [10]
Очевидно, отклонения свойств реального раствора от свойств идеального раствора определяются двумя слагаемыми: тепловым ( Я, - Я -, ид) и энтропийным ( Si - SjiHH. [11]
Ввиду невозможности определения свойств реальных растворов допускают заведомую неточность, считая раствор идеальным. Поэтому теория идеальных растворов позволяет с тем или иным приближением решать многие проблемы, связанные с реальными растворами. [12]
Усложняют химико-технологический процесс отклонение свойств реальных растворов и газов от идеальных, наличие примесей, ограничения в развитии скорости реакций; все это приводит к понижению выхода продукта. Вследствие этого пока еще недостаточно разработано полное научное прогнозирование на основе имеющихся теоретических положений и разработок оптимальных условий проведения новых процессов. [13]
Количественные закономерности, учитывающие отклонения свойств реальных растворов от свойств идеальных растворов, могут быть пока найдены лишь для отдельных классов растворов. Например, такие закономерности удалось установить для растворов неполярных неассоциированных жидкостей, для которых характерны небольшие отклонения от закона Рауля, а также для растворов теплота образования которых из компонентов равна нулю, и некоторых других-растворов. [14]
Количественные закономерности, учитывающие отклонения свойств реальных растворов от свойств идеальных растворов, могут быть пока найдены лишь для отдельных классов растворов. Например, такие закономерности удалось установить для растворов неполярных неассоциированных жидкостей, для которых характерны небольшие отклонения от закона Рауля, а также для растворов, теплота образования которых из компонентов равна нулю, и некоторых других растворов. [15]
Страницы: 1 2 3 4