Свойство - реальный раствор
Cтраница 3
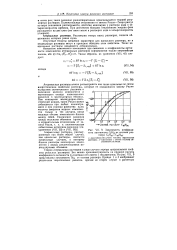 |
Зависимость коэффициента активности QHje от состава раствора C7Hle - CieH34. / - рассчитано без учета теплоты образования раствора. 2-рассчитано с учетом теплоты образования раствора. [31] |
Теория атермальных растворов в ряде случаев хорошо предсказывает свойства реальных растворов. Это можно проиллюстрировать на примере расчета коэффициента активности ( ft) гептана в его смесях с гексадеканом. На рис. VII, 9 представлена зависимость Irrfi от состава раствора. [32]
Понятие исключенного объема играет важную роль при рассмотрении свойств реальных растворов полимеров. Исключенный объем сегмента 3 определяет величину второго вириального коэффициента А2, величину разбухания клубка в хороших растворителях, а следовательно, существенно сказывается на гидродинамических свойствах и концентрационной зависимости многих свойств разбавленных растворов полимеров. Это приводит к усложнению интерпретации данных при определении структурных параметров линейных молекул и к значительным экспериментальным трудностям. [33]
К идеальным свойствам растворов и выводу на их основе свойств реальных растворов можно подойти путем проведения аналогии с предшествующим рассмотрением газов, причем в качестве критерия идеальности раствора может использоваться его соответствие закону Рауля. [34]
 |
Графическое изображение энергии Гиббса для регулярного раствора. [35] |
Часто, однако, модель регулярного раствора не может описать свойства реальных растворов, и приходится вводить второй параметр. [36]
 |
Графическое изображение положительного ( / и отрицатель о-го ( 2 отклонений от закона Рауля. [37] |
Коэффициент активности - безразмерная величина, она является мерой отклонения свойств реальных растворов от свойств идеальных растворов. [38]
Перспективность этого метода состоит в возможности описания единой схемой большого числа концентрационных зависимостей свойств реальных растворов, в том числе и термодинамических свойств. [39]
Избыточный химический потенциал - функция только состава и используется для измерения степени отклонения свойств реального раствора от свойств идеального раствора. [40]
В связи с этим формулы, выведенные для бесконечно разбавленных растворов, могут описывать свойства реальных растворов, если вместо аналитических концентраций в них подставлены действующие концентрации или активности компонентов. Физический смысл активности - это та условная концентрация, при которой рассматриваемый компонент, обладающий теми же свойствами, что и в бесконечно разбавленном растворе, сохраняет значения термодинамических функций, присущих реальному раствору. [41]
Значение коэффициентов активности не исчерпывается тем, что с их помощью можно установить отличие свойств реальных растворов от идеальных. [42]
Идеальные растворы подчиняются относительно простым законам и представляют удобные стандарты, с которыми можно сравнивать свойства реальных растворов. [43]
Теоретические расчеты коэффициентов активности основаны на представлениях, которые раскрывают природу сил, вызывающих отклонение свойств реальных растворов от свойств идеальных. Для расчета коэффициентов активности ионов используется теория Дебая - Хюккеля. По этой теории ион в растворе рассматривается как заряженная частица, окруженная ионной атмосферой преимущественно из противоположно заряженных ионов, а взаимодействие иона с ионной атмосферой имеет электростатический ( кулоновский) характер. [44]
Учитывая простоту закономерностей, которым подчинены идеальные растворы, а также сложность и подчас невозможность вычисления свойств реальных растворов, часто приходится допускать заведомую неточность и считать раствор идеальным. Поэтому теория идеальных растворов дает возможность с тем или иным приближением решать многие проблемы, связанные с растворами вообще. [45]
Страницы: 1 2 3 4