Свойство - бесконечно разбавленный раствор
Cтраница 1
Свойства бесконечно разбавленных растворов сохраняются и при конечных концентрациях, причем предельные концентрации можно определить лишь опытным путем. Экстраполяция свойств реальных растворов, найденных экспериментально, до бесконечно малых концентраций является методом проверки и обобщения экспериментальных данных. [1]
Изучение свойств бесконечно разбавленных растворов имеет практический интерес еще и по другой причине: в расчетах часто бывает необходимо производить экстраполяцию свойств, найденных опытным путем, - от конечных концентраций к бесконечно малым. [2]
Изучение свойств бесконечно разбавленных растворов имеет практический интерес еще и по другой причине: в расчетах часто бывает необходимо производить экстраполяцию свойств, найденных опытным путем, от конечных концентраций к весьма малым. [3]
Может показаться, что изучение свойств бесконечно разбавленных растворов представляет чисто теоретический интерес. [4]
Несмотря на логическую безупречность всех положений § 3, свойства бесконечно разбавленных растворов показывают, что эта схема не всегда удобна. В самом деле, для растворенного вещества в таком растворе соблюдается не закон Рауля, а закон Генри. Поэтому представляется вполне естественным и целесообразным построить термодинамику растворенного вещества на основе именно закона Генри. [5]
Если выбрать за стандартное состояние раствор одномоляльной концентрации со свойствами бесконечно разбавленного раствора и учесть, что мицеллообразование наблюдается при малых концентрациях ПАВ, то первым и последним членом в скобках уравнения ( VI. [6]
 |
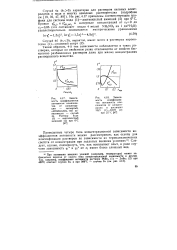
Зависимость коэффициентов активности компонентов от концентрации - случай 2а ( fci0, ч2. Расплав РЬВг2 - ZnBr2 при 500 С ( А, 0 4, Я, 4. In Yi 0 4 x24, ny2 0 4л. 24 - 0 533 х23. [7] |
Эти растворы уже при сравнительно больших концентрациях по своим свойствам совпадают со свойствами бесконечно разбавленного раствора. [8]
Если для упрощения анализа считать, что конденсированная фаза является чистым веществом, а газообразная обладает свойствами бесконечно разбавленного раствора, то уравнение ( 138, гл. [9]
В несимметричной системе стандартных состояний в качестве стандартного состояния растворенного вещества выбирают гипотетический одномоляльный раствор, который обладает свойствами бесконечно разбавленного раствора. [10]
Выберем в качестве стандартного состояния карбоновой кислоты, а также мономеров и димеров такой раствор, который обладает свойствами бесконечно разбавленного раствора. В последнем вся карбоновая кислота находится в виде мономера. [11]
Таким образом, 4 - й тип зависимости наблюдается в таких растворах, которые по свойствам резко отклоняются от свойств бесконечно разбавленных растворов даже при малых концентрациях растворенного вещества. [13]
MZ / M, отвечающий стандартному состоянию, за которое принимается гипотетический молярный раствор и аналогичная амальгама, обладающие свойствами бесконечно разбавленных растворов. [14]
За стандартное состояние принимают либо чистое вещество, либо, как в данном случае, гипотетический раствор, обладающий некоторыми свойствами бесконечно разбавленного раствора ( у 1 при С - - 0); ав и а0 - активности в водной и органической фазах. [15]
Страницы: 1 2 3 4