Свойство - коллоидная система
Cтраница 2
При объяснении свойств коллоидной системы необходимо учитывать не только размер частиц, но и наличие межфазной поверхности, обусловливающей возможность разнообразных адсорбционных явлений, а также различные химические реакции, которые могут протекать на поверхности частиц. [16]
Зависимость изменения свойств коллоидных систем от дисперсности частиц часто характеризуется максимумом-или минимумом, соответствующим определенной степени дисперсности. [17]
Однако изменения свойств коллоидной системы, являющейся неравновесной, связаны в первую очередь с теми изменениями, которые претерпевают отдельные коллоидные частицы от момента их образования и при протекающих в дальнейшем процессах старения. До настоящего времени обычно изучались процессы, протекающие во всей коллоидной системе в целом, так как вследствие экспериментальных трудностей нельзя было изучить поведение отдельной коллоидной частицы. [18]
При объяснении свойств коллоидной системы необходимо учитывать не только размер частиц, но и наличие межфазной поверхности, обусловливающей возможность разнообразных адсорбционных явлений, а также различные химические реакции, которые могут протекать на поверхности частиц. [19]
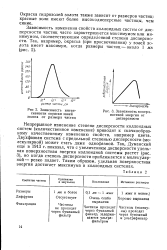 |
Зависимость поверхностной энергии от дисперсности. [20] |
Зависимость изменения свойств коллоидных систем от дисперсности частиц часто характеризуется максимумом или минимумом, соответствующим определенной степени дисперсности. [21]
Для изучения свойств коллоидных систем иногда очень важно получить монодисперсные системы. Получение таких монодисперсных золей основано на разделении процессов образования зародышей и их роста. При образовании зародышей возникают различные по величине, но в общем очень мелкие частицы. Если рост этих частиц происходит в одинаковых условиях, получается одинаковый прирост массы. Если последний велик по сравнению с массой зародышей, то разница в массах выросших кристалликов или капелек будет мала. [22]
Для уяснения свойств коллоидных систем было обращено большое внимание на поверхностные явления, имеющие место на макроскопических поверхностях раздела. Найденные закономерности были непосредственно перенесены на коллоидные системы типа эмульсий, суспензий, а дальше - на высокодисперсные золи. Здесь не надо забывать, что такое чисто механическое перенесение свойств макроповерхностей на ультрагюверхности коллоидных частиц не всегда возможно. [23]
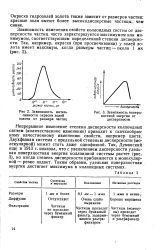 |
Зависимость поверхностной энергии от дисперсности. [24] |
Зависимость изменения свойств коллоидных систем от дисперсности частиц часто характеризуется максимумом или минимумом, соответствующим определенной степени дисперсности. [25]
Для объяснения свойств коллоидных систем необходимо учитывать наличие поверхности раздела фаз, обусловливающей возможность самых разнообразных адсорбционных явлений. Адсорбция является процессом концентрирования веществ на поверхности раздела фаз в результате молекулярного и электростатического взаимодействия. К явлениям адсорбции близки явления смачивания, также определяющиеся интенсивностью взаимодействия между молекулами различных веществ. Огромное значение для большинства физико-химических процессов имеет адсорбция из раствора. [26]
Другим примером использования свойств коллоидных систем может служить адсорбция суспензией метаоловянной кислоты значительных количеств фосфорной кислоты, чем пользуются для количественного отделения фосфат-ионов, осложняющих ход анализа смеси катионов ( см. гл. [27]
Другим примером использования свойств коллоидных систем может служить адсорбция суспензией метаоловянной кислоты значительных количеств фосфорной кислоты, чем пользуются для количественного отделения фосфат-ионов, осложняющих ход анализа смеси катионов. [28]
Другим примером использования свойств коллоидных систем может служить адсорбция суспензией метаоловянной кислоты значительных количеств фосфорной кислоты, чем пользуются для количественного отделения фосфат-ионов, осложняющих ход анализа смеси катионов. Можно упомянуть также о введении в анализируемую смесь некоторых органических веществ, как-то: желатины, крахмала, альбумина, агар-агара и др., увеличивающих стойкость коллоидных растворов и получивших название защитных коллоидов. [29]
Другим примером использования свойств коллоидных систем может служить адсорбция суспензией метаоловянной кислоты значительных количеств фосфорной кислоты, чем пользуются для количественного отделения фосфат-ионов, осложняющих ход анализа смеси катионов. [30]
Страницы: 1 2 3 4