Свойство - соль
Cтраница 1
Свойства солей R4NX легче объяснить, чем свойства галогенидов щелочных металлов, просто потому, что структурные взаимодействия 1 и 2 ( а возможно, и 6) преобладают над всеми остальными. Тем не менее наблюдается непрерывное изменение у при переходе от солей R4NX к галогенидам щелочных металлов. Исправление значений у галогенидов щелочных металлов на гидратации и взаимное высаливание сближает их значения, однако, как следует из рис. 6, порядок величин при этом остается неизменным. Отсюда окончательно следует, что структурные эффекты играют определенную роль в концентрационной зависимости термодинамических свойств галогенидов щелочных металлов. [1]
Свойство соли при хранении на воздухе расплываться, выветриваться или оставаться неизмененной обусловлено двумя факторами: давлением паров воды в воздухе и давлением паров гидрата и его насыщенного раствора. [2]
 |
Температуры плавления ( т. пл., температуры кипения ( т. кнп. [3] |
Свойства солей описаны также в работе: Gordon А. [4]
Свойства солей с многоатомными анионами, которые не являются акцепторами протонов ( соответствующие кислоты - сильные электролиты), объяснить труднее. [5]
Свойства солей с ранным количеством кислотного окисла значительно между собою различаются, но однч соль может быть превращена в другую прибавлением кислоты или основания весьма легко, и чем более элементов кислоты в соли, тем постояннее до известной степени раствор и сама образующаяся соль. Раствором вольфра-мовонатровой соли иногда пропитывают ткани, чтобы сделать их трудновоспламеняющимися, напр. [6]
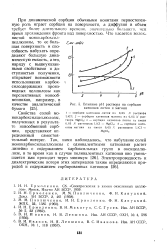 |
Влияние рН раствора на сорбцию катионов лития и магния. [7] |
Свойства солей мо-нокарбоксилцеллюлозы, полученных в результате ионообменной сорбции, представляют определенный самостоятельный интерес. [8]
Свойства солей азотистоводородной кислоты оправдывают рассмотрение азидной группы как псевдогалогена. [9]
Свойства нестехиометрических ион-радикальных солей очень близки к характеристикам комплексов с переносом заряда. [10]
Свойства солей органических кислот уже рассматривались ранее: пиролизом кальциевых солей получают альдегиды и кетоны ( стр. [11]
Свойством солей железа образовывать гидрат окиси, не-эастворимый в щелочкой и нейтральной среде, в завод -: кой технике пользуются для отделения железа во многих производствах. [12]
Сравнивая свойства солей этого вещества с солями известных дипиридилов, мы нашли, что они точно совпадают с солями а р-дипиридила. [13]
Какие свойства солей А ( III) вытекают из описания их малой устойчивости. [14]
Эти свойства солей серебра используются для его обнаружения. Все эти три этапа выполняются в указанной последовательности в одной и той же пробирке. [15]
Страницы: 1 2 3