Свойство - фтор
Cтраница 2
Хлор ( С1), атомная маюса 35 5, активный неметалл. Хлор повторяет свойства фтора. [16]
В процессе дальнейшей работы были выделены группы элементов, сходных между собой по свойствам. Действительно, сравнивая свойства фтора, хлора, брома и йода, мы видели, что эти элементы обладают близкими свойствами. Это дало право объединить их в одну группу и дать общее название - галогены. [17]
При изучении химических свойств элементов выявилось одно очень важное явление - они образуют естественные группы. Действительно, сравнивая свойства фтора, хлора, брома и иода, мы видели, что эти элементы обладают близкими свойствами; все они образуют соединения с водородом типа HR, где R - один из представителей этой группы; они непосредственно реагируют с металлами, образуя при этом типичные соли, например, NaF, NaCl, NaBr и KJ. Они образуют соли кислородсодержащих кислот, которые обладают сильными окислительными свойствами: КС1О, КВгО и KJO. [18]
В процессе дальнейшей работы были выделены группы сходных между собою по свойствам элементов. Действительно, сравнивая свойства фтора, хлора, брома и йода, мы видели, что эти элементы обладают близкими свойствами. Это дало право объединить их в одну группу и дать общее название - галогены. [19]
В процессе дальнейшей работы были выделены группы элементов, сходных между собой по свойствам. Действительно, сравнивая свойства фтора, хлора, брома и йода, мы видели, что эти элементы обладают близкими свойствами. Это дало право объединить их в одну группу и дать общее название - галогены. [20]
Ученый знал о разрушающих свойствах фтора, поэтому он изготовил электролизер целиком из платины, электроды - из ириди-ево-платинового сплава, а чтобы охладить пыл элемента-незнакомца, электролиз вели при - 23 С. [21]
Изменение химических свойств в ряду At-I-Br - C1 в основном определяется закономерным уменьшением размеров ns - и лр-ва-лентных орбиталей, но при переходе от хлора к фтору кроме того резко меняется состояние всей электронной оболочки, так как в атоме фтора отсутствуют остовные р-электроны и вакантные d - AO. Следствием этого является заметное отличие свойств фтора от свойств остальных элементов группы. Это делает молекулу F2 исключительно реакционноспособной: фтор непосредственно реагирует со всеми элементами, кроме Не, Ne и Аг, образуя в большинстве случаев соединения, в которых элементы находятся в максимально возможных степенях окисления: BiF5, SF6, OsF7, причем многие реакции со фтором идут уже при стандартных условиях. [22]
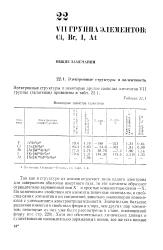 |
Некоторые свойства галогенов. [23] |
Так как в структуре их атомов недостает лишь одного электрона для завершения оболочки инертного газа, то эти элементы образуют отрицательно заряженный ион Х - и простые ковалентные связи-X. Значительно большие различия имеются в свойствах фтора и хлора, чем других пар элементов; некоторые из них уже были рассмотрены в главе, посвященной фтору ( см. стр. [24]
При переходе от фтора к йоду закономерно растут атомные и ионные радиусы, падает сродство к электрону и электроотрицательность, растут межъядерные расстояния молекул Г2 и соответственно падает их прочность. Вместе с тем, как будет показано ниже, свойства фтора ( как и других элементов второго периода) существенно отличаются от свойств электронных аналогов. [25]
Для атома лития ЭО принята равной 1 0; в ряду Be, В, С, N, О, F она постепенно возрастает и у фтора достигает 4 0 - это ее максимальная величина. Фтор - наиболее электроотрицательный элемент, что вполне соответствует свойствам фтора. ЭО водорода равна 2 1, у большинства металлов ЭО 1 7 или меньше. Разность ЭО атомов А и В ( XB - ХА) зависит от степени ионности связи. [26]
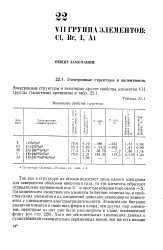 |
Некоторые свойства галогенов. [27] |
Так как в структуре их атомов недостает лишь одного электрона для завершения оболочки инертного газа, то эти элементы образуют отрицательно заряженный ион Х - и простые ковалентные связи - X. По химическим свойствам эти элементы типичные неметаллы, и свойства самих элементов и их соединений довольно закономерно изменяются с уменьшением электроотрицательности. Значительно большие различия имеются в свойствах фтора и хлора, чем других пар элементов; некоторые из них уже были рассмотрены в главе, посвященной фтору ( см. стр. [28]
Но наше объяснение опровергается при обращении к другим галогенам. Да, это действительно так, и тем не менее хлор не активнее фтора. Мы должны иметь в виду, что нельзя объяснить уникальность свойств фтора одной лишь причиной, необходим учет всех его особенностей. [29]
Так, в 1850 г. Макс Петтенкофер, профессор химии и гигиены из Мюнхена, расширил эти ряды, сопоставив и другие похожие друг на друга элементы, например азот, фосфор, мышьяк, сурьму. Он особенно подчеркивал, что свойства каждого из входящих в группу элементов типичны для всей данной группы; например, свойства фтора характерны для хлора, брома и иода или свойства кислорода характерны для серы, селена и теллура. [30]
Страницы: 1 2 3