Свойство - восстановитель
Cтраница 2
В ходе редокс-реакции окислитель принимает электроны и приобретает свойства восстановителя. В приведенном выше примере элементный иод превратился в иодид-ион, являющийся восстановителем. В этой же реакции восстановитель - сульфид-ион отдает электроны и превращается в элементную серу, обладающую свойствами окислителя. [16]
В отличие от высших низшие оксиды могут проявлять свойства восстановителей. Их сила как восстановителей уменьшается по периодам и группам. [17]
Форма кривой перед точкой эквивалентности определяется в основном свойствами восстановителя, а после точки эквивалентности - свойствами окислителя. Вблизи точки эквивалентности происходит резкий скачок редокс-потенциала. Кривая на других участках имеет незначительный уклон, так как потенциал медленно изменяется при титровании. [18]
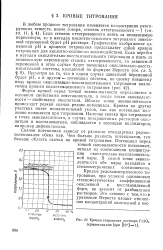 |
Кривая титрования раствора FeSC4 перманганатом ( при [ Н ] l. [19] |
Форма кривой перед точкой эквивалентности определяется в основном свойствами восстановителя, а после точки эквивалентности - свойствами окислителя. Вблизи точки эквивалентности происходит резкий скачок редокс-потенциала. Кривая на других участках имеет незначительный уклон, так как потенциал медленно изменяется при титровании. Наличие скачка при титровании в точке эквивалентности, в случае неокрашенных растворов окислителя и восстановителя, наблюдается с помощью индикаторов, например дифениламина. [20]
Для качественного и количественного определения аскорбиновой кислоты пользуются ее свойствами восстановителя и другими реакциями. Аскорбиновая кислота, например, дегидрогени-руется при освещении в присутствии метиленовой синей. [21]
ОН синего цвета, растворимое в воде и обладающее свойствами восстановителя. Это вещество рассматривают как соединение одновалентного никеля, и оно, очевидно, совершенно отлично по типу от карбонил-нитрозилов кобальта и железа. [22]
Благодаря большому сродству металлического А1 к кислороду алюминий обладает ярко выраженными свойствами восстановителя. Подробно изучил метод алюмотер-мии и предложил его применять для сварки деталей из железа Гольд-шмидт. [23]
Малая скорость восстановления достигается применением органических соединений, не обладающих свойствами восстановителей. В процессе серебрения эти соединения распадаются с образованием новых веществ, которые и являются собственно восстановителями. Винокурову [12], действие восстановителей основано на образовании из молекул восстановителя молекул формальдегида или других активных форм альдегидов с двухвалентным ненасыщенным атомом углерода, которые и служат восстанавливающим веществом. [24]
Химик имеет дело с водородом как с веществом, обладающим свойствами идеального восстановителя. [25]
В реакциях с сильными окислителями в кислой среде перекись водорода проявляет свойства восстановителя. [26]
Азотистый ангидрид, как и соответствующая ему азотистая кислота, проявляет свойства восстановителя и окислителя. [27]
В реакции с оксидом ртути ( II) муравьиная кислота проявляет свойства восстановителя. Эту реакцию применяют для идентификации муравьиной кислоты. [28]
Приведенные данные показывают, что в зависимости от условий: количества и свойств использованного восстановителя, а также рН среды, в которой проводится реакция - при восстановлении нитросоединений могут быть получены различные продукты. Почти все приведенные в схемах соединения вырабатываются промышленностью и имеют практическое значение. [29]
Химик имеет дело с водородом прежде всего как с веществом, обладающим свойствами идеального восстановителя. [30]
Страницы: 1 2 3 4