Свойство - идеальный газ
Cтраница 2
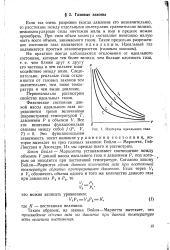 |
Изотермы идеального газа. [16] |
Первоначально рассмотрим свойства идеальных газов. [17]
Отклонения от свойств идеального газа и способность к конденсации параллельно изменяются для разных газов. В случае веществ с полярными молекулами значительно усиливаются и отклонения от свойств идеального газа и способность к конденсации. [18]
Наиболее близко свойствам идеального газа соответствуют достаточно разреженные газы. [19]
Смесь обладает свойствами идеального газа. [20]
Спирта сильно отличаются от свойств идеальных газов. Поэтому Ньютон и Додж [12] для сопоставления экспериментальных данных различных авторов ( табл. 1) произвели пересчет всех констант к нулевому давлению. [21]
Отклонения реальных газов от свойств идеального газа в общем увеличиваются с понижением температуры и с повышением давления. [22]
Чтобы установить для некоторых мольных свойств идеального газа их зависимости от температуры, выразим эти свойства через изобарную мольную теплоемкость. [23]
Однако при значительных отклонениях от свойств идеального газа, что имеет место при повышенных давлениях, а также при наличии явлений турбулентности, фактор градиента давления должен определяться иначе. [24]
Применим микроканоническое распределение к нахождению свойств идеального газа. [25]
Таким образом, для определения свойства идеального газа в состоянии равновесия требуется знать функцию распределения по скоростям. Для неидеальных газов или жидкостей необходима функция пространственного распределения; для установления свойств систем, не находящихся в равновесии, а изменяющихся во времени, необходимо использовать функции распределения по скоростям и пространственного распределения, которые сами являются функциями времени. [26]
Свойства реального газа отличаются от свойств идеального газа тем сильнее, чем выше давление в системе. Поэтому интегрирование уравнения (12.39) невозможно произвести для широкого интервала изменения давлений. [27]
Отступление свойств реальных газов от свойств идеальных газов обнаруживается не только при изучении сжимаемости газов, но также при изучении калорических свойств газов, например их теплоемкостей. [28]
Свойства реального газа отличаются от свойств идеального газа тем сильнее, чем выше давление в системе. Поэтому интегрирование уравнения (12.39) невозможно произвести для широкого интервала изменения давлений. [29]
Таким образом, для определения свойства идеального газа в состоянии равновесия требуется знать функцию распределения по скоростям. Для неидеальных газов или жидкостей необходима функция пространственного распределения; для установления свойств систем, не находящихся в равновесии, а изменяющихся во времени, необходимо использовать функции распределения по скоростям и пространственного распределения, которые сами являются функциями времени. [30]
Страницы: 1 2 3 4