Свойство - гидроксид
Cтраница 3
Этому постепенному переходу соответствует и повышение окислительного числа элементов, образующих гидроксиды. Такое же соответствие наблюдается при рассмотрении изменения свойств гидроксидов ( и оксид-гидроксидов) одного и того же элемента с разными окислительными числами. [31]
Этому постепенному переходу соответствует и повышение окислительного числа металлов, образующих гидроксиды. Такое же соответствие наблюдается при рассмотрении изменения свойств гидроксидов ( и оксид-гидроксидов) одного и того же металла с разным окислительным числом. [32]
Например, практика показала, что изучение зависимости свойств гидроксидов элементов от степени окисления и радиуса центрального атома требует неоправданно много времени. [33]
Например, практика показала, что изучение зависимости свойств гидроксидов элементов от степени окисления и радиуса центрального атома требует неоправданно много времени. И этот вопрос был исключен. [34]
Оксиды элементов, химически взаимодействуя с водой, способствуют смещению этого равновесия, в результате чего раствор становится либо кислым, либо щелочным. По этой причине гидроксиды являются характеристическими соединениями, поскольку свойства гидроксида определяют, в конечном итоге, принадлежность элемента к металлам или неметаллам. Следует, однако, подчеркнуть, что характеристическими в этом смысле свойствами гидроксиды обладают только в водных растворах. В других растворителях их кислотно-основные функции могут резко измениться. Например, оксид азота N2Or, с водой образует гидроксид HNO3, который в водном растворе является сильной кислотой. Это характеризует азот как типичный неметалл, a N2O5 как кислотный оксид. [35]
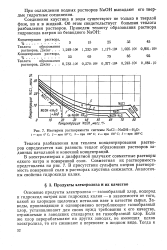 |
Изотермы растворимости системы NaCl-NaOH-РЬО. [36] |
В электролизерах с диафрагмой получают совместные растворы едкого натра и поваренной соли. В присутствии сульфата натрия растворимость поваренной соли в растворах каустика снижается. Аналогичны свойства гидроксида калия. [37]
Гидроксид алюминия амфотерен ( от греч. Амфо-терность - свойство гидроксида совмещать черты слабого основания и слабой кислоты - присуща гидроксидам р - и d - металлов и особенно ярко выражена у гидроксида алюминия. [38]
К одной из них добавить несколько капель раствора соляной кислоты, к другой - избыток раствора гидроксида натрия и перемешать. На какое свойство гидроксида бериллия это указывает. [39]
Следует отметить и отрицательные стороны ее. Кислотно-щелочная система еще недостаточно разработана; она пока ограничивается анализом катионов, предусмотренных программой аналитической химии педагогических институтов. Требуется более глубокое исследование свойств гидроксидов катионов четвертой и пятой групп и условий их осаждения и разделения. [40]
Образовавшийся осадок разделите на две части и к одной части осадка добавьте раствор кислоты, а к другой - щелочи. Какой вывод можно сделать относительно свойств гидроксида висмута. [41]
Как известно, гидрокси-ды обычно рассматриваются как продукты взаимодействия оксидов с водой независимо от того, наблюдается это взаимодействие в действительности или гидроксид может быть получен только косвенным путем. Гидроксиды являются характеристическими соединениями, поскольку свойства гидроксида определяют в конечном итоге принадлежность элемента к металлам или неметаллам. [42]
Здесь ясно виден постепенный переход от типичных оснований - гидроксидов калия и кальция - к хромовой и марганцовой кислотам. Этому соответствует и повышение окислительного числа металлов, образующих гидроксиды. Такое же соответствие наблюдается при рассмотрении изменения свойств гидроксидов ( и оксид-гидроксидов) одного и того же металла в разной степени окисления. [43]
При неравномерном распределении оксидов железа на металлической поверхности оборудования возникает своеобразная пара дифференциальной аэрации. Участки металла под локальным скоплением оксидов металлов играют роль анодов; поверхность металла с тонким слоем оксидов является катодом. Характерной особенностью этой коррозионной системы является тот факт, что она действует вследствие деполяризующих свойств гидроксида железа ( III), находящегося на поверхности металла - большого по площади катода. Для этого вида принято название ракушечная, или подшламовая, коррозия. [44]
Амфотерные свойства проявляют гидроксиды таких металлов, как цинк, хром, свинец и олово, а также упоминавшийся выше алюминий. Отклонения от этого правила возникают в тех случаях, когда элементы имеют более сложные электронные конфигурации внешних оболочек. Так, например, было бы опрометчиво сравнивать, амфотерные свойства гидроксида алюминия со свойствами гидроксида цинка, поскольку Al3 имеет 8-элек-тронный остов, тогда как цинк обладает 18-элек-тронным остовом. [45]
Страницы: 1 2 3 4