Химическое свойство - растворитель
Cтраница 1
 |
Влияние физических и химических свойств среды на электрохимические процессы. [1] |
Химические свойства растворителя могут оказывать более непосредственное влияние на сопряженные реакции Формально можно различить два типа воздействия Во-первых, растворитель может быть доЕюром или акцептором разчнчных частиц. Так, ври восстановлении ароматических углеводородов в водной среде вода служит донором протовюв Кислотный характер этого растворителя неизбежно оказывает преимущественное влияние на ход всех проводимых в нем процессов восстановления. Основный характер растворителя также может оказывать слияние. [2]
Первый и второй типы дифференцирующего действия растворителей связаны с химическими свойствами растворителей, а третий - с физическими. Установлены также три аналогичных типа дифференцирующего действия растворителей на силу оснований. [3]
Это влияние обусловлено физическими свойствами растворителя ( температурой кипения, дипольным моментом, диэлектрической проницаемостью), химическими свойствами растворителя [ нейтральным протонодо-норным или протоноакцепторным ( кислотным или основным) характером. [4]
Большинство растворителей уменьшает силу кислот, по сравнению с водой только аммиак и некоторые другие основные растворители несколько усиливает ее. Это уменьшение определяется химическими свойствами растворителей. Во всяком случае, уменьшение силы кислот связано не только с диэлектрической проницаемостью растворителя. Даже в формамиде, диэлектрическая проницаемость которого больше, чем у воды, сила кислот уменьшается на 1 - 2 единицы К. По влиянию на силу кислот растворители располагаются в последовательный ряд по своей основности; диэлектрические проницаемости хотя играют и подчиненную, но достаточно, существенную роль. Низкая диэлектрическая проницаемость пиридина, несмотря на его высокую основность, приводит к заметному уменьшению силы кислот. [5]
Большинство растворителей уменьшает силу кислот, по сравнению с водой только аммиак и некоторые другие основные растворители несколько усиливает кислоты. Это уменьшение определяется химическими свойствами растворителей. Во всяком случае уменьшение силы кислот связано не только с диэлектрической проницаемостью растворителя. Даже в формамиде, диэлектрическая проницаемость которого больше, чем у воды, сила кислот уменьшается на 1 - 2 единицы р / С. По влиянию на силу кислот растворители располагаются в последовательный ряд по своей основности; диэлектрические проницаемости хотя и играют подчиненную, но достаточно существенную роль - Низкая диэлектрическая проницаемость пиридина, несмотря на его высокую основность, приводит к заметному уменьшению силы кислот. [6]
Большинство растворителей уменьшает силу кислот, по сравнению с водой только аммиак и некоторые другие основные растворители несколько усиливает ее. Это уменьшение определяется химическими свойствами растворителей. По влиянию на силу кислот растворители располагаются в последовательный ряд по своей основности; диэлектрические проницаемости хотя играют и подчиненную, но достаточно существеннную роль. Низкая диэлектрическая проницаемость пиридина, несмотря на его высокую основность, приводит к заметному уменьшению силы кислот. [7]
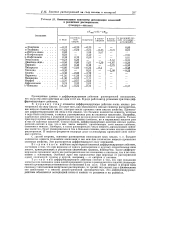 |
Относительные константы диссоциации оснований в различных растворителях. [8] |
Третий тип дифференцирующего действия состоит в том, что при попадании кпслоты или основания даже одной природной группы в растворители с низкой диэлектрической проницаемостью изменяется соотношение в их силе. Бели первый и второй типы связаны с химическими свойствами растворителя, то третий тип связан уже с физическими его свойствами - с низкой диэлектрической проницаемостью. Это дифференцирующее действие объясняется ассоциацией ионов и зависит от различия в их радиусах. [9]
Третий тип дифференцирующего действия состоит в том, что при попадании кислоты или основания даже одной природной группы в растворители с низкой диэлектрической проницаемостью изменяется соотношение в их силе. Если первый и второй типы связаны с химическими свойствами растворителя, то третий тип связан уже с физическими его свойствами - с низкой диэлектрической проницаемостью. Это дифференцирующее действие объясняется ассоциацией ионов и зависит от различия в их радиусах. [10]
Таким образом, уксусная кислота для кислот является дифференцирующим, а муравьиная - нивелирующим растворителем. Следует, впрочем, еще раз подчеркнуть, что роль диэлектрической проницаемости в нивелировании и дифференцировании силы электролитов проявляется столь заметно лишь когда химические свойства растворителей разнятся несущественно. [11]
Растворители с высокой диэлектрической проницаемостью способствуют нивелированию силы электролитов. В таких растворителях равновесная концентрация свободных ионов обусловлена ослаблением энергии электростатического взаимодействия между катионом и анионом в ионном двойнике. Химические свойства растворителя в данном случае играют второстепенную роль. [12]
Терпеновые растворители, добываемые из сосны, являются старейшими из растворителей, применяемых в лакокрасочной промышленности. В настоящее время их заменяют во многих покрытиях более дешевыми алифатическими углеводородными растворителями. Химические свойства терпено-вых растворителей делают их ценным сырьем для производства синтетических смол и других соединений. [13]
Выбор растворителя может существенно изменить направление реакции и равновесие ее. Тогда же обнаружилось, что химические свойства растворителя существенно влияют на поведение электролита в растворе. [14]
Однако, кроме такого дифференцирующего действия, имеются случаи, когда даже кислоты или основания одной природной группы, попадая в растворители с низкой диэлектрической проницаемостью, изменяют соотношение в своей силе. Если первый и второй типы связ-аны с химическими свойствами растворителя, то третий тип связан уже с физическими его свойствами - с низкой диэлектрической проницаемостью. Это дифференцирующее действие обязано ассоциации ионов и зависит от различия в их радиусах. [15]
Страницы: 1 2