Химическое физическое свойство - вещество
Cтраница 2
При данном определенном составе молекул взаимное расположение атомов в пространстве является вторым по важности фактором ( первый - последовательность химической связи атомов), определяющим химические и физические свойства вещества. Поэтому можно расширить бутлеровское понятие химического строения, включив в него также пространственное строение молекулы. В этом случае сохраняет силу положение, согласно которому сзойства вещества определяются его химическим строением. [16]
При данном определенном составе молекул взаимное расположение атомов в пространстве является вторым по важности фактором ( первый - последовательность химической связи атомов), определяющим химические и физические свойства вещества. Поэтому можно расширить бутлеровское понятие химического строения, включив в него также пространственное строение молекулы. В этом случае сохраняет силу положение, согласно которому свойства вещества определяются его химическим строением. [17]
Открытие изомерии выдвинуло перед химиками важнейшую задачу - изучить зависимость физико-химических свойств соединений от их состава и строения, поскольку исследования изомерных соединений наглядно показали, что химические и физические свойства веществ зависят не только от природы атомов и их числа, но и от расположения атомов в молекулах. [18]
С другой стороны, положительный заряд ядра определяет общее число электронов в атоме и, зная закономерность распределения электронов по уровням и подуровням в атоме, мы можем найти строение внешнего незаконченного электронного уровня, который в свою очередь будет определять химические и физические свойства веществ, построенных из данного вида атомов. [19]
 |
Неполная гибридизация орбиталей атома С. [20] |
С другой стороны, положительный заряд ядра определяет общее число электронов в атоме и, зная закономерность распределения электронов по уровням и подуровням в атоме, мы можем найти строение внешнего незаконченного электронного уровня, который, в свою очередь, будет определять химические и физические свойства веществ, построенных из данного вида атомов. [21]
Однако в последнем, внешнем слое, в котором находятся валентные электроны, число электронов не может быть больше восьми. Валентные электроны определяют химические и физические свойства вещества, так как легко вступают во взаимодействие с валентными электронами атомов других веществ. [22]
Здесь мы рассмотрим только важные для самой ядерной физики процессы ионизации и появления наведенной активности. Воздействие излучений на химические и физические свойства вещества, а также биологическое действие излучений будут рассмотрены ниже в гл. [23]
Попытки классифицировать элементы предпринимались издавна и завершились гениальным открытием Д. М. Менделеева, который в 1869 г. создал периодическую систему элементов. По закону периодичности - фундаментальному закону природы - химические и физические свойства веществ, образованных элементами, связаны прежде всего с электронными конфигурациями и величиной заряда ядра соответствующих элементов. Кроме общей классификации элементов, основанной на строении электронных конфигураций и закономерностях периодической системы, существует давнее традиционное разделение их на металлы и неметаллы. [24]
В обширной литературе по применению изотопов в химических исследованиях главное внимание уделяется методу меченых атомов в его многочисленных вариантах. Менее распространено использование для исследовательских целей различий в химических и физических свойствах веществ, отличающихся друг от друга только по своему изотопному составу. Между тем такие различия ( изотопные эффекты) могут дать существенные сведения о строении вещества и о механизме ряда процессов. Достаточно напомнить значение изотопных эффектов для создания современной теории сверхпроводимости металлов. Особенно богатые возможности скрыты в исследовании кинетических изотопных эффектов химических реакций, которым посвящена предлагаемая вниманию читателей монография известного шведского ученого Ларса Меландера. [25]
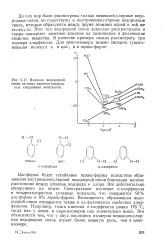 |
Влияние водородной связи на точку кипения водородных соединений неметаллов. [26] |
До сих пор были рассмотрены только межмолекулярные водородные связи, но существуют и внутримолекулярные водородные связи, которые образуются между двумя атомами одной и той же молекулы. Этот тип водородной связи довольно распространен и также оказывает заметное влияние на химические и физические свойства вещества. [27]
Старинное это определение вполне точно, но е очень ясно выражено. Мы называем молекулой наименьшее количество данного вещества, вступающее в химическую реакцию и тем самым ответственное за химические и физические свойства вещества. [28]
Это приводит к образованию молекулярных ассоциатов ( HjO, CjHsOH) или димерных молекул ( карбоновые кислоты) и к существенному влиянию на химические и физические свойства веществ. Возможно образование водородной связи и внутри молекулы, например, в о-нитрофеноле. [29]
Величайшее разнообразие химических свойств 103 элементов и в то же время периодичность этих свойств, позволившая создать периодическую систему, обусловлены законом природы, нашедшим свое выражение в принципе исключения. Если бы не действовал этот принцип, т.е. если бы последующие электроны в любом количестве могли занимать наиболее устойчивую орбиту в каждом атоме с п 1, тогда химические и физические свойства веществ изменялись бы совершенно одинаково с увеличением атомного номера и мир не характеризовался бы таким огромным разнообразием строения и состава, каким он характеризуется в действительности. [30]
Страницы: 1 2 3