Полученное значение - константа - скорость
Cтраница 1
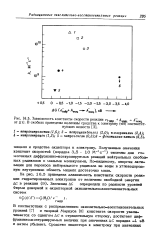 |
Зависимость константы скорости реакции е-гидр. Лш. ц - от Д G. В скобках приведены величины сродства к электрону ( эВ соответст. [1] |
Полученные значения констант скоростей ( порядка 3 5 10 М-1 с -) типичны для гомогенных диффузионно - контролируемых реакций нейтральных свободных радикалов с малыми молекулами. По-видимому, энергия активации для переноса нейтрального радикала из воды в углеводородную внутреннюю область мицелл достаточно мала. [2]
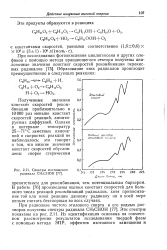 |
Спектры поглощения радикала СН3СНОН. [3] |
Полученные значения констант скоростей рекомбинации приблизительно в 10000 раз меньше констант скоростей реакций, лимитируемых диффузией. [4]
Полученное значение константы скорости крекинга изобутана очень близко к наблюдаемому экспериментально. [5]
Подставляя полученные значения констант скоростей в кинетические уравнения процесса, определяли соотношение скоростей окисления арсенопирита и пирита в равноценных условиях окисления. [6]
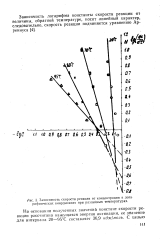 |
Зависимость скорости реакции от концентрации в логарифмических координатах при различных температурах. [7] |
На основании полученных значений констант скорости реакции рассчитана кажущаяся энергия активации, ее значение для интервала 20 - 95 С составляет 36 9 кдж / моль. [8]
А ] 3 / 2 и 10 5 е кт [ А ] 3 / 2 Полученные значения констант скорости и энергий активации вполне приемлемы. [9]
В наиболее благоприятных случаях, таких, как превосходные исследования изомеризации метилизоцианида [6], можно было считать полученные значения констант скорости достаточно надежными; однако эта система является исключением. Химическая активация дает активированные молекулы с узким распределением по энергиям, причем скорости реакций этих молекул можно измерить непосредственно. Спектроскопическое исследование химической активации, проведенное Норришем, Поляни и сотрудниками, значительно расширило наши представления о распределении по энергиям образующихся в реакции молекул, содержащих до трех или четырех атомов. Ниже мы рассмотрим реакции значительно больших молекул, чем те, которые были изучены ранее. Первым примером активированной молекулы, изученной специально с этой целью, был этан [7], образующийся при рекомбинации метильных радикалов. Образовавшаяся вначале молекула снова распадалась, если не была предварительно дезактивирована за счет соударений. Отсюда следовало, что скорость рекомбинации метильных радикалов, по-видимому, зависит от давления. Из этих исследований была получена несколько большая информация, чем можно было получить на основании изучения симметричного разложения этана. К сожалению, последнюю реакцию нелегко исследовать. [10]
Образование ТФК по реакциям ( 5) - ( 7) в дальнейшем не учитывали, так как они имеют второстепенное значение, что подтвердилось полученными значениями констант скоростей. [11]
Кинетика этой перегруппировки была изучена для 1 4 М растворов гек-са-метилацетона IB следующих кислотах: HF - SbFs ( 9: 1), HSO3F - SbFj ( 5: 1), HSO3F, H2SO4 и HF. Полученные значения констант скоростей незначительно отличаются друг от друга: 6 - 10 - 4, 1 0 - 10 - 3, 6 3 - 10 - 4, 3 5 - 10 - 4 и 2 3 - 10 - 4 соответственно. [12]
Обработка данных по окислительному дегидрированию изоами-ленов в изопрен [37] на железо-цинк-хромовом катализаторе производилась с помощью электронно-вычислительной машины при допущении, что реакция окислительного дегидрирования необратима и протекает по первому порядку и при избытке кислорода по нулевому порядку, если пренебречь конверсией углеводородов до Со и С02; также предполагалось, что изомеризация обратима и адсорбционные центры однородны в адсорбционном и каталитическом отношении. Полученные значения констант скоростей удовлетворительно согласовались с данными кинетических опытов с индивидуальными изомерами. [13]
 |
Экспериментальные условия роста кальцита в отсутствие добавок и расчетные константы скорости. [14] |
Приведенные значения были получены для одной и той же исходной суспензии кальцита, разбавленной до рабочего раствора перед началом каждой серии опытов. Относительно малые различия полученных значений констант скорости являются строгим доказательством надежности метода роста затравки. Незначительные различия констант скорости в разных сериях опытов для чистых растворов вызваны изменениями исходной суспензии затравки за время исследования. [15]
Страницы: 1 2