Электронное свойство - поверхность
Cтраница 2
Тем не менее известно, что при дроблении в кристаллической решетке могут образоваться различные дефекты и дислокации, что приводит к возникновению большого числа поверхностных состояний, способных резко изменить электронные свойства поверхности носителя. И, наконец, вызывает сомнения основной вывод работы о том, что переход 1 электрона проводимости из носителя на 10 000 атомов никеля может заметно изменить каталитическую активность последнего. [16]
Обнаруженная качественная связь величин электроотрицательности атомов примеси со знаком изменения работы выхода полупроводника указывает на преобладающее действие на ср образующихся твердых растворов внедрения или микрогетерогенных систем. Для ряда изученных систем электронографически установлено, что на поверхности СиО примеси образуют отдельную фазу. Это указывает на преобладающее влияние микрогетерогенных включений на электронные свойства поверхности. Модифицирующие добавки, увеличивающие ср СиО, повышают, а примеси, понижающие ср, уменьшают селективность процесса окисления. [17]
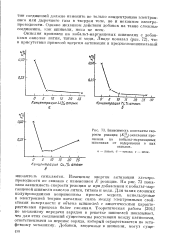 |
Зависимость константы скорости реакции ( уд окисления пропилена на кобальт-марганцевых шпинелях от содержания в них окислов. [18] |
Изменение энергии активации электропроводности не связано с изменением Е реакции. На рис. 73 показана зависимость скорости реакции w при добавлении к кобальт-марганцевой шпинели окислов лития, титана и меди. Для таких сложных полупроводников неприменимы простые модели, используемые в электронной теории катализа; связь между электронными свойствами поверхности и объема шпинелей с кинетическими характеристиками процесса более сложная. Теоретическая работа [294] по механизму передачи зарядов в решетке шпинелей показывает, что для этих соединений существенны расстояния между катионами, ответственными за перенос заряда, который осуществляется по эстафетному механизму. [19]
При изучении кинетики электродных процессов весьма важно применять очищенные электролиты, равно как и электроды. Типичный монослой на электродной поверхности содержит около 1015молекул - см-2 ( при полном заполнении), или 10 - 9 моль - см-2. Иногда даже малое заполнение поверхности существенно влияет на кинетику электродных процессов, блокируя каталитические центры, изменяя электронные свойства поверхности или влияя на осаждение и растворение посредством блокирования выступов и изломов, участвующих в процессах распространения поверхностных дефектов. Ситуация становится критической, если поверхность электрода подвергается действию примесей в течение времени, достаточного для ее заполнения, даже в том случае, когда концентрация примесей в растворе не превышает микромолей. [20]
Сопоставление рис. 3 и таблиц 4 и 5 показывает, что в катализаторах окисления углеводородов почти всегда присутствуют переходные элементы. Рогинский еще в 1935 г. [70] высказал предположение, что присутствие в катализаторе незаполненных й-оболочек в элементах, входящих в состав катализатора, способствует образованию дополнительных связей твердого тела с адсорбирующимися молекулами. Каталитический процесс складывается из ряда последовательных элементарных актов, которые сопровождаются разрывом и образованием связей в молекулах реагирующих веществ и электронными переходами между твердым телом - катализатором и реагирующими молекулами. Следовательно, электронные свойства поверхности катализаторов влияют на каталитические адсорбционные процессы. [21]
Свойства поверхности образцов изучаются путем приложения небольшого напряжения ( 0 01 - 10 В) и регистрации туннельного тока в зазоре ( примерно несколько атомных диаметров) между электропроводящим острием ( зондом) и исследуемой поверхностью металлов, полупроводников и других проводящих материалов. Туннельный ток зависит от химического состава и особенностей рельефа. Эта информация дополняется данными спектроскопических измерений. Полученные результаты характеризуют топографию, химические и электронные свойства поверхности. [22]
Окислительная переработка углеводородов издавна привлекала внимание исследователей как одно из основных направлений органического синтеза. Кислород вступает с углеводородами в разнообразные реакции присоединения, замещения, деструктивного и полимеризационного окисления. Металлические катализаторы, используемые в окислительном катализе, как правило, бывают покрыты более или менее тонким полупроводниковым чехлом. В случае достаточно толстого слоя ( порядка десятков атомных слоев) химические и электронные свойства поверхности будут целиком определяться свойствами этой пленки; в случае тонкого слоя ( порядка нескольких атомных слоев) свойства поверхности будут определяться как пленкой, так и металлической подложкой, а именно, пленка будет влиять на концентрацию носителей тока ( электрон или дырка) на поверхности. Поэтому в окислительном катализе механизм процесса на металлах и полупроводниках имеет много общего. На всех окислительных катализаторах, при широких вариациях условий проведения процесса, с различным соотношением скоростей протекают реакции неполного окисления, приводящие к образованию кислородсодержащих ценных продуктов, и реакция глубокого окисления, приводящая к образованию углекислого газа и воды. Ввиду обилия типов окислительных реакций сравнительная характеристика контактов представляет трудную задачу. [23]
По данным Трепнела [95], процесс хемосорбции кислорода на различных металлах и при различных температурах протекает так быстро, что кинетику процесса не удается измерить; это указывает на очень малую величину энергии активации хемосорбции. После быстрой хемосорбции начинается медленное поглощение кислорода металлом. Такое поглощение для никеля, меди и некоторых других металлов сопровождается образованием окислов этих металлов. Для благородных металлов ( платина, серебро) медленный процесс поглощения приводит к растворению кислорода в приповерхностных слоях. Калиш [74] показала, что при адсорбции кислород внедряется в приповерхностные слои платины в количестве, равном десяткам монослоев. В последнее время Темкин и Кулькова [75 ] исследовали сорбцию кислорода на пористом серебре при 250 и пришли к выводу, что через 185 час. Таким образом, кислород легко внедряется в приповерхностные слои благородных металлов ( платина, серебро), резко изменяя электронные свойства поверхности. [24]
Страницы: 1 2