Термохимическое свойство
Cтраница 2
Как и алюминий, магний обладает высокими термохимическими свойствами. [16]
В термохимии накоплены обширные данные о различных термохимических свойствах разных химических соединений и элементарных веществ. Эти данные можно найти в соответствующих справочных изданиях, причем в настоящее время в большинстве справочников они выражены в термохимических калориях. [17]
В общих сводках не имеется данных по термохимическим свойствам щавелевоуксусной кислоты. [18]
Модель независимых связей дает также предсказания о термохимических свойствах. [19]
 |
Зависимость диполь-ных моментов от силовых констант. [20] |
Аналогичный характер изменений для исследованных членов ряда имеют и термохимические свойства. Изменение порядков и энергетики связей нитрогрупп должно быть взаимосвязано с изменением зарядов на атомах, а это в свою очередь не может не отразиться на величинах ди-польных моментов молекул. Действительно, значения ди-польных моментов молекул нитросоединений ( только для симметричных молекул) меняются также в порядке предложенного ряда. [21]
Для элегаза по сравнению с другими газообразными средами характерны специфические термохимические свойства, рассмотренные ниже. [22]
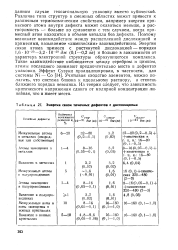 |
Энергия связи точечных дефектов с дислокациями. [23] |
Различие типа структур в смежных областях может привести к различным термохимическим свойствам, например энергия примесного атома внутри дефекта может оказаться меньше, а растворимость - больше по сравнению с тем случаем, когда примесный атом находится в объеме металла без дефекта. Поэтому возникает взаимодействие между расщепленной дислокацией и примесями, называемое химическим взаимодействием. [24]
Расхождение этой величины с опытной вызвано, по-видимому, особыми термохимическими свойствами 2 3-диметилбутана. Молекула имеет ось симметрии 2-го порядка. [25]
Еще раньше, в 1881 г., Бертло14, изучая термохимические свойства хлоратов и перхлоратов, доказал, что превращение хлората калия в перхлорат происходит с выделением тепла. Исходя из этого, он установил, что перхлораты значительно более стабильны, чем соответствующие им хлораты. [26]
Свентославский ( 1908 г.) разделил органические соединения по их термохимическим свойствам на насыщенные и ненасыщенные. Парафины - отмечал он - являются единственными представителями тел, атомные связи которых доведены до полноты своего-насыщения, и в этих соединениях мы встречаем закон постоянства теплот образования атомных связей [ 179, стр. [27]
Особенностью выполнения исследований является использование массивов справочных и других известных данных о термохимических свойствах неорганических веществ для последующего выявления различных коррелятивных связей и функций, а также моделей твердых идеальных растворов продуктов взаимодействия и методологии термодинамического моделирования, развитых нами ранее. Монография содержит информацию только о разработках авторов и не претендует на полный обзор состояния исследований в этом направлении в мире. В шести главах книги описаны процедуры выполнения исследований, приведены выявленные закономерности, численные зависимости или методы расчета свойств. Всего представлено около 10 опробованных новых методов оценки А / / 98, 5 98 С 298 темпеРатУР кон - груэнтного плавления для неорганических веществ. По нашим данным, погрешности при использовании этих методов не превышают погрешности определения указанных свойств с применением современных экспериментальных способов. [28]
Мы располагаем результатами значительного числа измерений электрохимических свойств неводных растворов, но данные по термохимическим свойствам этих систем до последних лет почти отсутствовали. До 1950 г. можно было назвать только несколько работ, в которых при одной температуре и в ограниченной зоне концентраций определены теплоты растворения некоторых щелочно-галоидных солей в нескольких органических растворителях и в смесях метанола и этанола с водой. [29]
Мы располагаем результатами значительного числа измерений электрохимических свойств неводных растворов, но данные по термохимическим свойствам этих систем до последних лет почти отсутствовали. До 1950 г. можно было назвать только несколько работ, в которых при одной температуре и в ограниченной зоне концентраций определены теплоты растворения некоторых щелочно-галогенид-ных солей в нескольких органических растворителях и в смесях метанола и этанола с водой. [30]
Страницы: 1 2 3 4