Каталитическое свойство - фермент
Cтраница 1
Затем каталитические свойства фермента, особенно его способность связывать субстрат, были изменены путем сайт-специфической модификации. Так, трео-нин-51 был заменен на Яланин. Это привело к двукратному; увеличению связывания субстрата, видимо, из-за невозможности образования водородной связи между этим остатком и тирозил-аденилатом. При замене аланина проливом нарушается конфигурация молекулы фермента, но способность к связыванию субстрата увеличивается в сто раз, так как облегчается его взаимодействие с гистидином-48. Сходные сайт-специфичные изменения: были получены в р-лактамазе, и обычно они сопровождались инактивацией фермента. Замена серина-70 на цистеин приводит к образованию 3-тиоллактамазы, константа связывания у которой не отличается от таковой для природного фермента, но. Тем не менее активность этого мутантного фермента в отношении некоторых активированных цефалоспоринов не меньше исходной активности или даже превышает ее; эти белки также-более устойчивы к действию протеаз. [1]
В каталитических свойствах ферментов определенную роль играют ионы металлов. [2]
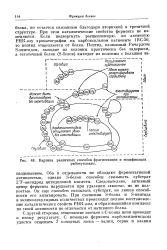 |
Картина различных способов фрагментации и модификации. [3] |
При этом каталитические свойства фермента не изменяются. Если подвергнуть расщепленную, но активную РНК-азу хроматографии на карбоксильном катионите IRC-50, то пептид отщепляется от белка. [4]
Кроме гетерогенного варианта ИФА применяют и другой, основанный на различиях в каталитических свойствах ферментов в свободном виде и в связанном. Его реализуют в гомогенных условиях, т.е. без отделения комплексов АГ-АТ. [5]
Значение константы р для этой реакции равно 1.95. По всей вероятности, имидазольное кольцо гистидина ответственно за каталитические свойства фермента липазы, с помощью которой осуществляется гидролиз липидов и других сложных эфиров. На этой основе был сделан вывод [6], что энзимати-ческий гидролиз менее чувствителен к электронной структуре фенилацетата, чем катализ с помощью одного имидазола. Это объясняется способностью фермента стабилизировать заряды, в результате чего распределение электронов в энзим-субстратном комплексе оказывается менее чувствительным к влиянию заместителей в фенильном радикале. [6]
Рентгенограммы кристаллических ферментов, полученные к настоящему времени, ясно демонстрируют все эти возможности, и они заслуживают самого пристального внимания исследователей, пытающихся объяснить каталитические свойства ферментов. [7]
В опытах Анфисена ( 1961) было установлено, что при разрыве дисульфидных мостиков в молекуле рибонуклеазы наступает полная потеря ферментативных свойств, но затем, после стояния и воздействия кислорода, восстанавливаются мостики, структура и каталитические свойства фермента. [8]
Уникальные каталитические свойства ферментов обусловлены двумя особенностями их структуры: многофункциональным характером активного центра и способностью к конформационным переходам. [9]
Известен ряд цитохромов, из которых наиболее изучены и получены в очищенном состоянии четыре, обозначаемые латинскими буквами, a, b, GI и с и цитохромоксидаза, или а3, называемая также теми новым дыхательным ферментом. Каталитические свойства геминовых ферментов обусловлены присутствием в их молекуле железа, которое, принимая и отдавая-электроны, попеременно восстанавливается и окисляется. [10]
Процессы ассоциации без сомнения играют одну из наиболее важных ролей в биохимии. Начальная степень связывания субстрата оказывает значительное влияние на каталитические свойства фермента. Важную роль играют специфические комплексы цепей нуклеиновых кислот или антител с антигенами. [11]
Цитохромы и цитохромоксидаза - ферменты геминовой природы. Они имеют почти одинаковую простатическую группу, но различные белковые компоненты. Каталитические свойства геминовых ферментов связаны с входящим в их молекулу железом, которое принимает и отдает электроны, изменяя при этом свою валентность, попеременно восстанавливаясь и окисляясь. Перенос электронов заканчивается с образованием цитохромоксидазы, способной реагировать непосредственно с кислородом. [12]
В организме человека и животных большинство реакций протекает при участии белковых катализаторов - ферментов. С повышением температуры скорость биохимических реакций соответственно возрастает. При высоких же температурах ( 50 - 60 С) каталитические свойства ферментов утрачиваются вследствие термоденатурации белка, и скорость реакций резко замедляется. Таким образом для химических процессов, протекающих в организме, выявляется так называемый температурный оптимум, который для теплокровных животных лежит в интервале примерно 36 - 42 С. [13]
После установления пространственной структуры этого фермента с помощью рентгеноструктурного анализа высказывалась точка зрения, что гидроксигруппа этого остатка принимает участие в подаче протона на атом азота гидролизуемой пептидной связи и одновременно в удалении протона от молекулы атакующей воды. Однако, когда методом сайт-специфичного мутагенеза была осуществлена замена этого остатка тирозина на фенилаланин, оказалось, что каталитические свойства фермента практически не изменились. [14]
У простых ферментов каталитическую функцию осуществляют непосредственно белки. В реакции с субстратом принимает участие не вся полипептидная цепь, а всего лишь несколько аминокислотных остатков, как правило, расположенных на значительном удалении друг от друга в полипептидной цепи. В процессе формирования третичной структуры происходит их сближение и стабилизация при помощи дисульфидных или множественных слабых связей. Денатурация нарушает связи, стабилизирующие третичную структуру, активный центр разрушается, и каталитические свойства фермента полностью или частично подавляются. [15]
Страницы: 1 2