Кислотное свойство - спирт
Cтраница 2
Кислотные свойства спиртов определяются способностью к про-тонизации атома водорода гидроксильной группы. Последняя обусловливается не только разницей в электроотрицательностях между атомами кислорода ( 3 5) и водорода ( 2 1), но и природой радикала. Содержание в последнем электронодонорных алкиль-ных групп, особенно у углерода, связанного с гидроксилом, уменьшает кислотность спирта и, наоборот, - введение электро-ноакцепторных заместителей увеличивает ее. [16]
Кислотные свойства спиртов выражены очень слабо. Со щелочными и щелочноземельными металлами спирты образуют солеобразные вещества - алкоголяты. При отщеплении воды от спиртов в зависимости от их строения и условий реакций образуются простые эфиры, алкены или же смеси этих соединений. Для спиртов характерна реакция этерифика-ции с карбоновыми кислотами, в результате которой получаются сложные эфиры. [17]
Кислотные свойства спиртов выражены очень слабо. [18]
Указанными кислотными свойствами спиртов объясняется тот факт, что реактивы Гриньяра разлагаются спиртами. Спирты протопируют карбанион-ный центр реактива Гриньяра, что и приводит к разрушению реактива. [19]
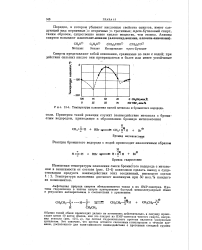 |
Температуры плавления смесей метанола и бромистого водорода. [20] |
Порядок, в котором убывают кислотные свойства спиртов, имеет следующий вид: первичные вторичные третичные; / npe / n - бутиловый спирт, таким образом, существенно менее кислое вещество, чем этанол. [21]
 |
Температуры плавления смесей метанола и бромистого водорода. [22] |
Порядок, в котором убывают кислотные свойства спиртов, имеет следующий вид: первичные вторичные третичные; трет-бу-тиловый спирт, таким образом, существенно менее кислое вещество, чем этанол. [23]
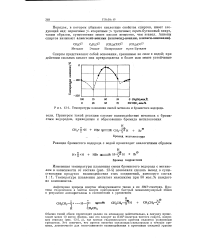 |
Температуры плавления смесей метанола и бромистого водорода. [24] |
Порядок, в котором убывают кислотные свойства спиртов, имеет следующий вид: первичные вторичные третичные; тгфет-бутиловый спирт, таким образом, существенно менее кислое вещество, чем этанол. [25]
В этом же ряду уменьшаются кислотные свойства спиртов. [26]
Поляризация связи О - Н позволяет говорить о кислотных свойствах спиртов. Поляризация связи О - Н также является причиной образования в спиртах и их водных растворах водородных связей. [27]
Если же ввести в радикал электроноакцепторные группы или атомы, то кислотные свойства спиртов значительно усиливаются. Например, спирт ( СЕ3) зС - ОН за счет электронооттягивающего действия атомов фтора становится настолько кислым соединением, что способен даже вытеснять угольную кислоту из ее солей. [28]
Если же ввести в радикал электроноакцептораые группы или атомы, то кислотные свойства спиртов значительно усиливаются. Например, спирт ( СР3) зС - ОН за счет электронооттягивающего действия атомов фтора становится настолько кислым соединением, что способен даже вытеснять угольную кислоту из ее солей. В данном случае это влияние является не непосредственным, а осуществляется через систему атомов: С - - С - - О. [29]
Кислотные свойства спиртов, обусловленные подвижностью атома водорода гидроксильной группы, зависят от значения индуктивного влияния алкильного радикала, связанного с гидроксильной группой: чем меньше электронодонорное влияние алкильного радикала на кислород гидроксильной группы, тем сильнее кислотные свойства спиртов. [30]
Страницы: 1 2 3