Электрохимическое свойство
Cтраница 1
Электрохимические свойства и влияние на них стехиомет-рического состава перовскитов исследованы в работе [61], из данных которой можно сделать заключение о невысокой анодной стойкости этих композиций при электролизе растворов хлоридов. [1]
Электрохимические свойства окислов азота изучены сравнительно мало. В качестве индикаторного электрода используется Pt-электрод. [2]
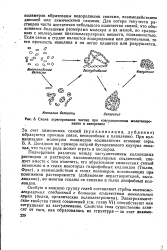 |
Схема агрегирования частиц при коагуляционном желатинировании и синерезисе. [3] |
Электрохимические свойства таких соединений ( см. главу VI) способствуют или затрудняют их застудневание. [4]
Электрохимические свойства полиакрилонитрильных 1волокон характеризуются высоким отрицательным зарядом на - их поверхности. В водной среде потенциал достигает 41 мВ, что способствует ускорению адсорбции катионных красителей и исключает поглощение красителей анионного типа. В зависимости от условий и состава раствора заряд волокна может изменяться в широких пределах. На величину потенциала волокна влияют концентрация красителя, электролита и поверхностно-активных веществ в растворе, температура и рН среды. [5]
Электрохимические свойства тонких слоев платины и катализ перекиси водорода на них. [6]
Электрохимические свойства гладких электролитически осажденных слоев платиновых металлов. [7]
Электрохимические свойства железа можно характеризовать следующими данными: нормальный равновесный потенциал железа - 0 44 В относится к процессу Fe - Fe и реализуется при активном процессе растворения железа. Равновесный потенциал процесса образования трехвалентных ионов Fe - Fe3 заметно менее отрицателен и равен - 0 036 В. Подобный процесс протекает при медленном растворении железа из пассивного состояния. В окислительных условиях железо обычно имеет заметно более положительный электрохимический потенциал в связи с большей или меньшей степенью его пассивации. [8]
Электрохимические свойства ОППЭ практически не отличаются от свойств обычных золотых и платиновых электродов. Химическая стойкость пленок довольно высока: платиновые пленки можно было удалить только в результате окисления, выделения водорода или восстановления Hg2 - noHOB; нормальная процедура отмывки и очистки, кипячение в течение нескольких секунд в концентрированной азотной кислоте, погружение на 12 час. Золотые пленки разрушались при обработке 0 1 М соляной или азотной кислотами. [9]
Электрохимические свойства свинца и олова похожи. На катоде металлы выделяются без заметной поляризации, с высоким выходом по току и склонны к образованию дендритов. [10]
Электрохимические свойства стеклоуглерода мало зависят от температуры карбонизации. [11]
Электрохимические свойства ДСК-электрода № 789 приведены на фиг. [12]
Электрохимические свойства астатина изучены весьма слабо, что объясняется отсутствием весовых количеств этого элемента. Природа электродных процессов, а также состав выделяющегося на электродах соединения астатина не были установлены. Выделение на катоде наблюдается в том случае, когда в растворе находятся бихромат-ионы, в присутствии которых, как было показано в работах [6,23], образуется одновалентный катион астатина. В том случае, когда астатин находится в растворе в элементарном состоянии или после окисления персульфатом, выделения на катоде не наблюдается. [13]
Электрохимические свойства системы превращают первичное распределение тока во вторичное. Различие между первичным к вторичным распределением тока определяется всеми теми факторами, которые воздействуют на появляющуюся при осаждении металла поляризацию. Поляризация повышается с увеличением плотности тока. Следовательно, на выступающих местах катода, на которых преобладает повышенная плотность тока, поляризация больше, чем на участках с меньшей плотностью тока. Так как поляризация может быть принята как включенное добавочное сопротивление, то в результате ее влияния плотность тока на выступающих местах катода уменьшается в значительно большей мере, чем на других участках. [14]
 |
Первичное распределение тока при различной форме электродов. [15] |
Страницы: 1 2 3 4