Электрохимическое свойство
Cтраница 2
Электрохимические свойства системы превращают первичное распределение тока во вторичное. [16]
Электрохимические свойства веществ непосредственно не связаны с их оптическими и ядерно-физическими свойствами. Поэтому в тех случаях, когда количественное определение разделенных на топком слое сорбента веществ оптическими и ядерно-физическими методами детектирования почему-либо затруднено, целесообразно использование электрохимических методов детектирования. [17]
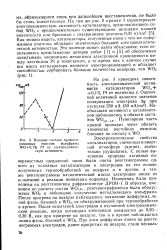 |
Влияние состава промоти-рованных окислов вольфрама WO 0 1 % Pt на электрохимическую активность. [18] |
Электрохимические свойства катализаторов, спеченных в инертной атмосфере ( аргон), значительно ухудшались. С целью выяснения природы активных поверхностных соединений нами были сняты рентгенограммы одного из исходных катализаторов и электродов на его основе, полученных термообработкой на воздухе и в аргоне, а также рентгенограммы каталитической массы электродов после их испытаний в реакции ионизации водорода. Измерения были проведены на рентгеновском дифрактометре ДРОН-1. [19]
Электрохимические свойства никеля довольно своеобразны. По справочным данным, стандартный электродный потенциал никеля равен - 0 250 В. [20]
 |
Разность потенциала границ з рен я компромиссного потенциала коррозии напряженных и ненапряженных термически обработанных сплавов в зависимости от длительности выдержи в 1 М растворе Nad. [21] |
Электрохимические свойства сегрегации: или выделений относительно матрицы, которые приводят в этих сплавах к межкри-сталлитным поражениям, исследовали в. Доиг и Эдингтон [10] использовали микроэлектроды для измерения локальных потенциалов коррозии на границах, зерен для А1 - Mg и А1 - Си сплавов и их. [22]
Электрохимические свойства цинка становятся важными, когда цинковое покрытие разрушается независимо от способа разрушения металла при экспозиции. В этом случае цинк, находящийся на поверхности стали, растворяется ( корродирует), защищая при этом от коррозии основной металл. Более того, продукты коррозии обычно заполняют нарушения в покрытиях и тем самым предотвращают коррозию стали. [23]
Электрохимические свойства ДСК-электрода № 789 приведены на фиг. [24]
 |
Первичное распределение тока при различной форме электродов. [25] |
Электрохимические свойства системы превращают первичное распределение тока во вторичное. [26]
Электрохимические свойства катионообменных мембран определяются главным образом составом полимерного материала, используемого для их изготовления. [27]
Электрохимические свойства титановых сплавов определяются преимущественно свойствами их главного компонента - титана. Равновесный электрохимический потенциал титана по отношению к водородному электроду равен - 1 63 В, что свидетельствует о его высокой термодинамической активности. Стационарные потенциалы титана в большинстве водных сред намного положи-тельнее; в морской воде при 25 С этот потенциал равен 0 09 В [177], что указывает на меньшую электрохимическую активность титана в данных условиях по сравнению с железом и на высокую стойкость его пассивного состояния. [28]
Электрохимические свойства применяемых мембран определяют максимальную допустимую разницу концентраций между обессоливаемым и концентрируемым потоками. На практике отношение скоростей обессоливаемых и рассольных потоков может изменяться в пределах от 3: 1 до 10: 1, так что изменение концентраций в этих потоках будет соответственно обратно пропорционально этим отношениям. Образование осадка может также ограничивать максимальную степень концентрирования, которую можно допустить в камерах рассола. [29]
Электрохимические свойства металлической поверхности изменяются в результате электрополирования. В большинстве случаев потенциал е - приобретает более положительные значения, поверхность пассивируется, облагораживается и становится более коррозион-ностойкой. [30]
Страницы: 1 2 3 4