Связи - атом - углерод
Cтраница 2
Наиболее стабильная конфигурация свободных радикалов может осуществляться в трех случаях: связи атома углерода, содержащего неспаренный электрон, лежат в одной плоскости ( как в ионе карбония), составляют тетраэдр или образуют промежуточную конфигурацию - плоскопирамидальную. В то же время энергия, необходимая для перевода такой пирамиды в плоскую или тетра-эдрическую конфигурацию, по-видимому, очень мала. [16]
Для правильного расположения молекулы углевода необходимо так преобразовать проекцию Фишера, чтобы связи атомов углерода с эндоциклическим кислородом были направлены по вертикали. В формуле I это достигается одновременным циклическим поворотом всех заместителей у атома С5, что, как известно, не изменяет конфигурации. Далее следует расположить цикл горизонтально, поместив кислород в правый дальний угол, и разместить заместители таким образом, чтобы группы, стоящие в формуле II слева от углеродной цепи, оказались наверху. Она является исходной для конформационного анализа молекул углеводов. [17]
Если такой газ нагреть с добавлением особых веществ - катализаторов или сжать с очень большой силой, то вторые связи атомов углерода освобождаются и присоединяют к молекуле ближайшую соседнюю. Так образуются длиннейшие цепи, состоящие из тысяч звеньев молекул мономера. [18]
Кекуле пришел к понятиям о четырехвалентное углерода и о связи между составными частями молекул химического соединения, в частности о связи атомов углерода между собой. Однако, находясь на правильном пути, Кекуле не смог отказаться от жераровских представлений и полагал, что для одного и того же соединения возможно несколько рациональных формул в зависимости от того, какие превращения этого соединения они выражают. [19]
Для того чтобы различить обе системы связей, связи ближнего атома углерода продолжают до пересечения в центре круга, а связи удаленного атома углерода оканчивают на окружности. [20]
Процессы полимеризации и поликонденсации нельзя считать законченными в момент изготовления самого полимера или изделия из него, так как остающиеся двойные и незамкнутые связи атомов углерода ( радикалы) могут еще вступать во взаимодействие, увеличивая этим постепенно коэффициент полимеризации, а следовательно, изменяя и механические свойства. [21]
В случае алкилгалогенидов, спиртов, альдегидов и кетонов, карбоновых кислот, нитросоединений в реакциях могут затрагиваться С - Н - связи атомов углерода, соседних с несущим функциональную группу. [22]
Гораздо труднее ответить на вопрос, какие силы удерживают два совершенно одинаковых атома; в простейшем случае это вопрос о связи атомов водорода в молекуле Н2, в более сложном случае - вопрос о связи атомов углерода в решетке алмаза. При решении этих вопросов в квантовой механике вбодйтся представление о так называемых обменных силах, или, вернее, обменной энергии. Гейзенберг ввел - эту обменную энергию при теоретическом исследовании вопроса о большом различии между энергиями три-плетных и сингулетных термов гелия, которые в соответствии с модельными представлениями могут различаться лишь параллельным и антипараллельным положением спинов обоих электронбв. Малой магнитной энергии двух магнетонов далеко не достаточно, чтобы объяснить это различие. Но если электроны различаются между собой, то наряду с определенным решением имеется второе решение, принадлежащее тому же собственному значению, отличающееся от первого только тем, что в нем оба электрона обменены между собой. Таким образом, в этом отношении система является вырожденной, и любая - линейная комбинация этих решений также представляет собой решение. Причем в этом случае, так же как в § 1, нужно найти такие комбинации, которые при введении возмущения дают новые собственные функции. Возмущением можно считать энергию электростатического взаимодействия обоих электронов, которой обычно пренебрегают. Если теперь использовать теорию возмущений то мы получим два сильно различающиеся между собой возмущенных собственных значения для двух линейных комбинаций, относящихся к параллельным и антипараллельным спинам. [23]
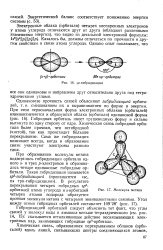 |
Молекула метана. [24] |
Электронные облака ( орбитали) четырех неспаренных электронов у атома углерода отличаются друг от друга ( обладают различными значениями энергии), что видно из детальной электронной формулы: l & 2sL2p ] e2py2pz - Казалось бы, должны отличаться по прочности и другим свойствам и связи атома углерода. [25]
В таких формулах указаны только связи между атомами углерода и связь углерода с гидроксильной группой ОН. Связи атомов углерода с водородом и кислорода с водородом опущены. Наглядность изображения последовательности соединения атомов не теряется, но формулы становятся менее громоздкими. На практике пользуются, как правило, сокращенными формулами. [26]
Атомы углерода бензола С6Н6 образуют правильный шестиугольник. Связи атомов углерода с водородом идут от всех вершин шестиугольника. Все атомы расположены в одной плоскости. [27]
Фенопласт или новолак Цепи-образованные между углеродными атомами, могут быть линейными, представляющими собой спиралевидные сложные системы. Связи атомов углерода между собой могут давать также сетчатую или пространственную конфигурацию полимера. Длина цепи определяется коэффициентом полимеризации л, который представляет собой среднюю, статистическую величину и, чем острее пик распределения этой величины, тем стабильнее свойства данного полимера. [28]
У лантанидов и актинидов незаполненной оказывается третья снаружи оболочка - / - орбиталь; d - и / - орбитали также могут участвовать в образовании связей. Связи атома углерода с переходными элементами непрочные и поэтому соединения, образовавшиеся только за счет внешних электронов, неустойчивы. Особенно малоустойчивы соединения алифатического ряда. Производные ароматического ряда более стабильны. [29]
Атомы углерода бензола С Нв образуют правильный шестиугольник. Связи атомов углерода с водородом идут от всех вершин шестиугольника. Все атомы расположены в одной плоскости. [30]
Страницы: 1 2 3 4