Двойные тройные связи
Cтраница 1
 |
Виды химических двухэлектронных связей. а, б, в - о - связь. е, д - я-связь. [1] |
Двойные и тройные связи в случае двухэлектронного приближения рассматриваются как состоящие из отдельных двухэлектронных связей. При этом некоторые из последних могут быть а-связями, другие - я-связями. [2]
Двойные и тройные связи обладают большими рефракциями связей, так как тг-электроны легче поляризуются, чем а-электроны. Таким образом, двойные и тройные связи легко идентифицировать при помощи молекулярной рефракции. Даже d - связи в напряженных циклах, как, например, в циклопропане и циклобутане, обладают большими рефракциями связей ( см. табл. 11), что может служить для идентификации этих циклов. [3]
Двойные и тройные связи обладают бблыпими рефракциями связей, так как тт-электроны легче поляризуются, чем ст-электроны. Таким образом, двойные и тройные связи легко идентифицировать при помощи молекулярной рефракции. Даже а-связи в напряженных циклах, как, например, в циклопропане и циклобутане, обладают бблыпими рефракциями связей ( см. табл. 11), что может служить для идентификации этих циклов. [4]
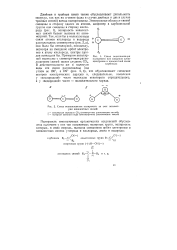 |
Схема возникновения.| Схема возникновения полярности за счет асимметрии ковалентных связей. [5] |
Двойные и тройные связи также обусловливают дипольность молекул, так как их я-связи ( одна в случае двойных и две в случае тройных связей) всегда поляризованы. Электронные облака я-связей смещены в сторону одного из атомов, например в карбонильной группе они смещены в сторону кислорода ( рис. 1), полярность ковалентных связей бывает вызвана их асимметрией. Так, если бы в молекуле воды связи атомов кислорода и водорода располагались симметрично ( рис. 2, а), она была бы неполярной, поскольку, несмотря на смещение орбит электронов к атому кислорода, центры зарядов совпадали бы. [6]
Двойные и тройные связи также обусловливают дипольность молекул, так как ( С их п-связи ( одна в случае двойных и две в случае тройных связей) всегда поляризованы. Схема возникновения смещены в сторону кислорода ( рис. 4), полярности при смещении полярность ковалентпых связей бывает вызвана их асимметрией. Так, если бы в молекуле воды связи атомов кислорода и водорода располагались симметрично, она была бы неполярной, поскольку, несмотря на смещение орбит электронов к атому кислорода, центры зарядов совпадали бы. В действительности в молекуле воды эти связи расположены под углом не 180, а 105 ( см. рис. 2, а), что обусловливает смещение центров электрических зарядов и, следовательно, появление у кислородной части молекулы некоторого отрицательного, а у водородной - положительного заряда. [7]
 |
Образование л-связи двумя р-облаками. [8] |
Двойные и тройные связи имеют общее название: кратные связи. [9]
Двойные и тройные связи называются кратными связями. [10]
Двойные и тройные связи имеют силовые постоянные, приблизительно в два и три раза соответственно большие. Поэтому, согласно уравнению ( 21 - 1), атомы, соединенные двойными или тройными связями, имеют более высокие частоты колебаний, чем те, что соединены одинарной связью. Атомы водорода колеблются с более высокими частотами, чем более тяжелые атомы, в связи с влиянием массы водорода на значение приведенной массы осциллятора. Такое простое объяснение, однако, применимо не ко всем молекулам, особенно к крупным и довольно сложным, однако, оно дает предпосылки для изучения и аналитического использования молекулярных колебаний. [11]
Двойные и тройные связи характеризуются большей сближенностью соответствующих атомов углерода по сравнению с простой связью. Так, в случае двойной связи расстояние С С составляет около 1 33 А, в случае тройной связи расстояние СС равно 1 20 А, тогда как у соединений с простыми связями расстояние С - С равняется 1 53 - 1 54 А. [12]
Двойные и тройные связи особенно чувствительны к каталитическому гидрированию. [13]
Двойные и тройные связи углерод - азот в таких соединениях, как нитрилы, изонитрилы, имины и др., обычно гидролизуются в мягких условиях. [14]
Двойные и тройные связи характеризуются большей сближенностью соответствующих атомов углерода по сравнению с простой связью. [15]
Страницы: 1 2 3 4