Двойные тройные связи
Cтраница 2
Двойные и тройные связи в эфирах кротоновой и тетроловой кислот выступают в роли М - заместителей, ведущих к повышению электронной плотности на карбонильном углероде. Способность олефиновых или ацетиленовых групп проявлять себя в роли - / - заместителей в этих случаях не обнаруживается, так как концевая метальная группа своим - - / - эффектом почти нейтрализует указанное влияние. [16]
Двойные и тройные связи обозначают, как обычно. [17]
Ординарные, двойные и тройные связи имеют силовые постоянные, приблизительно равные 5, 10 и 15 - 105 дин / см соответственно. [18]
Но двойные и тройные связи между одинаковыми атомами ( СС, СС, NN) имеют обычно средние или слабые полосы валентных колебаний, а в симметричных структурах такие колебания вообще не активны в ИК-спектрах. [19]
Но двойные и тройные связи между одинаковыми атомами ( СС, CMC, NN) имеют обычно средние или слабые полосы валентных колебаний, а в симметричных структурах такие колебания вообще не активны в ИК-спектрах. [20]
Но двойные и тройные связи между одинаковыми атомами ( СС, СзС, NN) имеют обычно средние или слабые полосы валентных колебаний, а в симметричных структурах такие колебания вообще не активны в ИК-спектрах. [21]
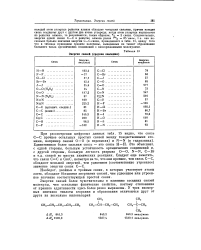 |
Энергии связей ( средние значения. [22] |
Наоборот, двойные и тройные связи, в которых участвуют атомы азота, обладают большими энергиями связей, чем удвоенное или утроенное значение соответствующей простой связи. [23]
Молекулы, содержащие двойные и тройные связи между соседними атомами, при столкновении часто стремятся раскрыть л-связн и за счет освободившихся электронов образовать между собой сг-связь. При этом из нескольких малых молекул образуется одна большая - полимер. Все рассмотренные виды связи возникают в том случае, когда электроны взаимодействующих атомов имеют антипараллельные спины и могут находиться в области связывания между ядрами атома. [24]
Непредельные углеводороды имеют двойные и тройные связи между атомами углерода в молекулах. От предельных углеводородов они отличаются меньшим числом атомов водорода в молекуле. Непредельные углеводороды подразделяют на три группы. [25]
Вещества, имеющие двойные и тройные связи, обладают способностью уплотняться. При этом происходит соединение большого количества одинаковых молекул по месту двойных связей с образованием новых, более сложных по строению молекул. [26]
 |
Схема образования ковалентпых связок в молекуле метана. [27] |
Непредельные углеводороды имеют двойные и тройные связи между атомами углерода в молекулах. От предельных углеводородов они отличаются меньшим числом атомов водорода в молекуле. Непредельные углеводороды подразделяют на три группы. [28]
Прямое действие озона на двойные и тройные связи известно давно. Эта реакция применяется в органической химии для определения структуры органических соединений. Несмотря на огромные знания, накопленные в этой области, механизм озонирования был объяснен лишь недавно. В настоящее время точно установлено, что озон разрывает двойные связи. Рихе и других [17] была выяснена структура озонидов. [29]
К функциональным группам относятся двойные и тройные связи в молекулах. [30]
Страницы: 1 2 3 4