Фосфодиэфирные связи
Cтраница 2
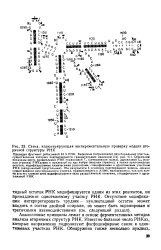 |
Схема, иллюстрирующая экспериментальную проверку модели вторичной структуры РНК. [16] |
Аналогичные принципы лежат в основе ферментативных методов анализа вторичных структур РНК - Известно большое число РНКаз, которые направленно гидролизуют фосфодиэфирные связи в одно-тяжевых участках РНК. [17]
Препараты рибонуклеазы, полученные из разных сырьевых источников, мО гут иметь различные свойства [1, 2], Большинство из них специфически расщепляет фосфодиэфирные связи, образованные пиримидиновыми нуклеотидами, и не действует на связи между пуриновыми нуклеотидами. Препараты рибонуклеазы отличаются различной чувствительностью к активаторам, ингибиторам и субстратной специфичностью. [18]
Исследование, проведенное с использованием в качестве субстратов различных синтетических нуклеотидо - ( Р - - Ы) - аминокислот ( пептидов), показало, что гидролитические ферменты, расщепляющие пептидные или фосфодиэфирные связи ( проназа, панкреатическая РНК-аза, фосфодиэстераза), не расщепляют фосфоамидную связь в этих соединениях. [19]
При щелочном гидролизе РНК образуется смесь нуклеозид-2 - фосфатов X и нуклеозид - З - фосфатов XI, что согласуется как со структурой V ( R OH) для РНК, так и с изомерной ей структурой, содержащей 2 - 5 -фосфодиэфирные связи, и с любой структурой, в которой 2 - 5 - и 3 - б - фосфодиэфирные связи чередуются в произвольном порядке. Исследование механизма щелочного гидролиза РНК показало185, что этот результат объясняется участием гидроксильной группы при С-2 остатка рибозы в процессе расщепления фосфодиэфирнои связи и промежуточным образованием ну-клеозид-2 / 3 -циклофосфатов XII, которые расщепляются далее с образованием смеси X и XI ( более подробно - см. гл. [20]
Молекулы Т.к. построены из повторяющихся звеньев, представляющих собой полиолы или гликозилполиолы, соединенные фосфодиэфирными связями. Фосфодиэфирные связи в поли ( глицерофосфатных) Т.к. ( ф-ла I) могут соединять положения 3 2 или 1 3, а в поли ( рибитфосфатных) Т.к. установлены только связи 1 5; строение маннит - Т.к. изучено недостаточно. Гидрок-сильные группы полиолов могут быть гликозилированы ( остатками глюкозы, галактозы, маннозы. В нек-рых Т.к. остатки Сахаров, гликозилирующих полиол, включены в главную цепь полимера. [21]
Второй метод состоит в частичном метилировании полинуклеотида диметилсульфатом и последующей обработке гуанил - РНК-азой. Фосфодиэфирные связи остатков гуанозина, подвергшихся метилированию по N-7, не расщепляются. [22]
Одна из них, с оптимумом рН около 6 0, гидролизует все фосфоэфирные связи в РНК с образованием нуклеозид-2 3 -циклических фосфатов. Она гидролизует фосфодиэфирные связи только между соседними пиримидиннуклеотидами с образованием богатых пуринами олиго-нуклеотидов. [23]
Эти данные позволили сделать вывод, что расщепление фосфодиэфирных связей при кислотной деградации ДНК происходит по негликозилированным дезоксирибозильным остаткам, образующимся в результате отщепления пуриновых оснований ( см. гл. При этом фосфодиэфирные связи у негли-козилированного дизоксирибозильного звена расщепляются как по 3 -, так и по Б - положениям. Было также показано122, что 3 - и 5 -монобензиловые эфиры пуриновых дезоксинуклеотидов в условиях кислотного гидролиза отщепляют пурин и бензилфосфат, в то время как соответствующие пиримидиновые производные в этих условиях относительно устойчивы. [24]
Из ферментов, катализирующих гидролитический распад РНК, наиболее изучены рибонуклеазы I. Они гидролизуют фосфодиэфирные связи внутри молекулы РНК. Получен в гомогенном состоянии из плесневого гриба рода Aspergillus фермент гуанилрибонуклеаза, катализирующая эндонуклеолитическое расщепление РНК. [25]
Рибонуклеаза Tj - специфическая рибонуклеаза, впервые обнаруженная в ас-пергилловых грибах. Она специфически гидролизует фосфодиэфирные связи в РНК между З - ГМФ - и 5 - ОН-группами соседних нуклеотидов. Этот весьма термостабильный и устойчивый в кислой среде фермент широко применяется ( благодаря специфичности действия) при исследовании первичной структуры РНК. [26]
 |
Фосфорилированные полисахариды в структуре клеточных стенок ( а и в. [27] |
Как следует из рис. 2.4, фосфодиэфирные связи в одной из цепей направлены от атома углерода в 5 -подожении в дезо-ксирибозе одного нуклеотида к атому углерода в З - положении другого нуклеотида. В комплементарной цепи эти же связи направлены от 3 -к 5 -углероду. Такая противоположная направленность комплементарных цепей обеспечивает стабильность структуры ДНК. [28]
 |
Схема, иллюстрирующая экспериментальную проверку модели вторичной структуры РНК. [29] |
Известно большое число РНКаз, которые направленно гидролизуют фосфодиэфирные связи в одно-тяжевых участках РНК - Обнаружено также несколько нуклеаз. [30]
Страницы: 1 2 3 4