Сильный водородные связи
Cтраница 1
Сильные водородные связи имеют место и в некоторых соединениях фтора, например во фтористом водороде. [1]
Сильные водородные связи придают аммиаку диполярный характер, вследствие чего в нем облегчается образование заряженных частиц типа катионов, а также радикал-анионов, анионов и дианио-нов. Известно, что катионы сольватированы как в протонных, так и в диполярных апротонных растворителях, но по способности соль-ватировать анион эти два типа растворителей заметно различаются. И хотя формально по классификации Паркера аммиак относится к протонным растворителям, значительно большая его способность, чем, например, гидроксилсодержащих растворителей, сольватиро-вать анионные реагенты позволяет считать его, по существу, апро-тонным растворителем. Важно также то, что протонироваться аммиаком могут лишь относительно основные анионные частицы. В случае необходимости кислотность среды может быть увеличена добавлением соединений - доноров протонов, таких как кислые углеводороды, спирты или вода. Все это создает основу для проведения в аммиаке реакций, в которых важную роль играют интер-медиаты анионного типа. [2]
Сильные водородные связи имеют место и в некоторых соединениях фтора, например во фтористом водороде. [3]
Сильные водородные связи, образуемые ДМСО с растворенными в нем фенолами, замедляют обмен настолько, что в отсутствие катализаторов протоны воды и группы ОН фенола дают разделенные узкие сигналы ЯМР. В диоксане, образующем более слабые водородные связи, обмен протекает быстрее и разделенные линии воды и группы ОН уширены. [4]
Следует различать слабые и сильные водородные связи. Некоторые водородные связи следует отнести к промежуточной группе; для них смещение частоты составляет 500 - 700 см-г, расстояния О О варьируют в пределах 2 6 - 2 7 А. [5]
Индол также образует сравнительно сильные водородные связи. Катрицкий [182] составил таблицу и рассмотрел довольно значительные смещения частот, которые наблюдаются при переходе от раствора к твердой фазе. [6]
В случае с HF сильные водородные связи приводят к аномально высокой температуре кипения по сравнению с остальными галогеноводородами. [7]
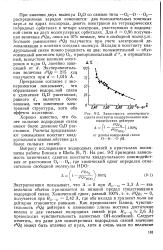 |
Зависимость химического сдвига константы квадрупольного взаимодействия дейтерия. [8] |
Хорошо известно, что более сильные водородные связи имеют более длинные ОХ0 расстояния. Расчеты предсказывают уменьшение констант квад-рупольного взаимодействия для более сильных связей. [9]
В полярных системах, очевидно, образуются сильные водородные связи между водой и молекулами растворителя. Это можно проиллюстрировать на примере системы, содержащей диоксан. В разбавленных растворах во многих неполярных растворителях, например в четыреххлористом углероде, вода может находиться в свободном состоянии, если не образуются межмолекулярные водородные связи. [10]
За исключением тех случаев, когда существуют сильные водородные связи, полосы валентных колебаний NH обычно довольно узкие даже для конденсированных фаз. Эта полезная особенность полос не может служить, однако, безотказным тестом. У первичных аминов теоретически имеются две полосы, соответствующие симметричным и антисимметричным валентным колебаниям. В конденсированных фазах часто наблюдается больше двух полос. Полосы могут быть плохо разрешены, но уже сама их вероятная множественность помогает отличать их от полос ОН. [11]
В кристаллах с бесконечными цепными анионами встречаются сильные водородные связи внутриионного типа. Надежно установлено наличие таких связей в структуре пектолита Ca2Na ( HSi309) [ 1, стр. [12]
В соответствии с расчетными и опытными данными различают слабые и сильные водородные связи. [13]
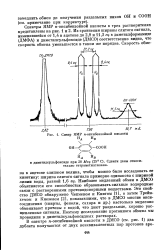 |
Спекр ЯМР га-оксибензойной кислоты. [14] |
Наиболее медленный обмен в ДМСО объясняется его способностью образовывать сильные водородные связи с растворенными протонодонорными веществами. Это свойство ДМСО обнаружено Чепменом и Кингом [1], а затем Трейн-хемом и Кнезелем [2], показавшими, что в ДМСО многие окси-соединения ( спирты, фенолы, сахара и др.) настолько медленно обменивают протоны с водой, что дают раздельные, хорошо расщепленные сигналы. [15]
Страницы: 1 2 3 4