Более длинные связи
Cтраница 1
Более длинные связи, обозначенные NI - О3 и NI - О5, имеют длину около 3 04 А. Более короткие связи, обозначенные Nt - O2 и Ni - O4, имеют длину около 2 93 А. [1]
Еще более длинные связи Те - 5мост обнаружены в мостиковом катионе [ Te2 ( tu) 6 ] 4 ( к), где к тому же, вероятно, имеет место понижение симметрии, что, по-видимому, пока не имеет убедительного объяснения. [2]
Еще более длинные связи Ag-С ( - 3 2 А) объединяют группы. [3]
Иными словами, высшие d - орбиты обусловливают более длинные связи. [4]
Соединения с конфигурацией искаженного тетраэдра, например Сгр2, имеют четыре короткие связи в плоскости ху и две более длинные связи, расположенные перпендикулярно этой плоскости. Четыре короткие связи описываются гибридными dsp2 - орбиталями, подобными орбиталям, образующимся в плоском квадратном комплексе. [5]
Это приводит к тому, что группы в экваториальной плоскости отталкиваются слабее, чем группы на оси г, и, так же как в случаях марганца и двухвалентного хрома, наблюдаются более длинные связи в направлении г. В очень многих кристаллических соединениях меди последняя окружена четырьмя группами в одной плоскости и еще двумя группами на несколько большем расстоянии, над и под этой плоскостью. Гидра-тированный медноаммиачный сульфат содержит квадратные группы Cu ( NH3) 4, связанные еще с двумя молекулами воды, одна из которых находится сверху, а другая - снизу. В предельном случае две группы по оси z уже не связаны с медью и возникает плоский квадратный комплекс. Однако в сильном поле более стабильной из двух орбит dv оказывается орбита dZ4, на которой и находятся оба электрона. У комплексов такого типа также наблюдаются искажения правильного октаэдрического расположения, но они гораздо меньше тех, которые имеют место при несимметричном заполнении с - орбит. Это, несомненно, связано с тем фактом, что орбиты d, направлены между линиями связей, а не вдоль этих линий. [6]
Интересно отметить, что более короткие связи С-О встречаются в тех случаях, когда кислород связан только с одним атомом углерода и не связан больше с каким-либо другим атомом, в то время как более длинные связи С-О встречаются в тех случаях, когда кислород связан еще с каким-либо третьим атомом. Этот эффект находит довольно простое объяснение: по-видимому, когда вся способность кислорода к образованию связей расходуется только на один атом, образующаяся связь оказывается прочнее и короче, чем в тех случаях, когда кислород одновременно связан с двумя атомами. [7]
В этом случае становится понятным, что в тригональной бипирами-де ( АВ5), где аксиальные атомы взаимодействуют с тремя лигандами, расположенными нормально к оси молекулы, а экваториальные атомы-с двумя нормальными лигандами и с двумя, чьи связи расположены под углом 120 ( см. рис. 5), аксиальные атомы должны иметь более длинные связи, чем экваториальные. В молекулах АВ4Е неподеленная е - - пара всегда занимает экваториальное положение из-за меньшего суммарного отталкивания, по сравнению с аксиальным расположением. [8]
Однако атом серы, связанный с кислородом, находится на большем расстоянии от своих соседей ( - 2 2 А), чем другие атомы кольца. Эти более длинные связи b и с ( на рис. 16Л, а) сопоставимы по длине с наиболее протяженной связью а в самой молекуле S. Ее фрагмент SsO может быть описан как геометрический изомер свободной молекулы, но длина связи S-О возрастает от 1 48 А в свободной молекуле до 1 55 А в SsO-SbCls, а длины соседних связей S-S уменьшаются при таком переходе от 2 20 до 2 11 А. [9]
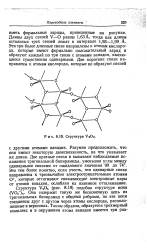 |
Структура VaOt. [10] |
Длины двух связей V-О равны 1 63 А, тогда как длины остальных трех связей лежат в интервале 1 93 - 1 99 А. Эти три более длинные связи направлены к атомам кислорода, которые имеют формально положительный заряд и образуют каждый по три связи с атомами ванадия, являющиеся существенно одинарными. [11]
Посредством связей ппа b двойные иепи присоединены к рути-лоподобным цепочкам с образованием слоев в направлении, указанном стрелками на рис. 26.13. Эти слон соединены более слабыми связями d в трехмерную структуру. Все пять более коротких связен лежат по одну сторону от атомов Sn, координационный полиэдр которого можно описать как одпошапочную три-гопальную призму. Две более длинные связи направлены к атомам одного ребра. [12]
Все галогенэтаны имеют близкие по величине... Предполагают, что возрастание барьера вращения по, сравнению с - этаном обусловлено ва. Более тяжелые галогены имеют большие ван-дер-ваальсрвььрд-диусы, но и более длинные связи, так что суммарный эффект для всех галогенов является величиной относительно постоянной. [13]
 |
Милскуляриые структуры B4Cl4 ( a, BjCl8 ( б и В9С19 ( а. [14] |
Связи В - С1 ординарные ( 1 70 А), а длина связей В-В ( также 1 70 А) соответствует кратности около 2 / з, если принять для атома бора радиус 0 8 А и использовать уравнение Полинга ( разд. Этот полиэдр ( рис. 24.8 6) ближе к додекаэдру ( бис-дисфеноиду), чем к квадратной антипризме, однако наблюдается значительный разброс в длинах связей В-В. Четыре более длинные связи ( рис. 24.8, а) находятся в интервале 1 93 - 2 05 А, остальные-1 68 - 1 84 А. [15]
Страницы: 1 2