Атомные связи
Cтраница 3
Например, при сгорании цинка в атмосфере кислорода образуется оксид, в котором электроны, осуществляющие атомные связи, оттянуты в сторону атомов кислорода, в результате чего на последних появляется избыток отрицательного заряда, равный его недостатку на атомах цинка. [31]
По современным научным воззрениям, процесс сгорания углеродистых материалов происходит в две стадии: вначале разрываются атомные связи, а затем каждый атом окисляется в отдельности. Чем меньше требуется энергии на разрыв межатомных связей, тем больше реакционная способность кокса. [32]
Во-вторых, как указывалось выше, при сгорании углеводородов, углеродистых материалов и алмаза сначала разрываются все атомные связи, а затем сгорает каждый атом в отдельности. Энергия углерод-углеродной связи в углеводородах отличается от энергии этой связи в графите и алмазе по данным Н. Н. Семенова [1] только на ккал / молъ, а по позднейшим данным [6] только на 2 6 - 2 7 ккал / молъ, что лежит в пределах возможной ошибки определения. [33]
Во-вторых, как указывалось выше, при сгорании углеводородов, углеродистых материалов и алмаза сначала разрываются все атомные связи, а затем сгорает каждый атом в отдельности. Энергия углерод-углеродной связи в углеводородах отличается от энергии этой связи в графите и алмазе по данным Н. Н. Семенова [1] только на ккал / моль, а по позднейшим данным [6] только на 2 6 - 2 7 ккал / молъ, что лежит в пределах возможной ошибки определения. [34]
Срединное положение азота, имеющего справа и слева лишь по два десмогена, не дает ему возможности осуществить атомные связи с повышенной энергией, которые, как это видно на рис. 213, появляют-ся-лишь у третьего и четвертого соседа, а не у второго и первого. [35]
Низкие коэффициенты испарения отмечаются в тех случаях, когда при переходе из твердого состояния в газообразное ( или наоборот) разрываются стабильные атомные связи. [36]
По современным научным воззрениям, процесс сгорания углеводородов, углеродистых материалов и даже алмаза проходит в две стадии: вначале разрываются все атомные связи, а затем каждый атом сгорает в отдельности. Это означает, что чем меньше требуется энергии на разрыв межатомных связей в молекуле данного соединения, тем больше его реакционная способность. [37]
По современным научным воззрениям, процесс сгорания углеводородов, углеродистых материалов и даже алмаза проходит в две Стадии: вначале разрываются все атомные связи, а затем каждый атом сгорает в отдельности. Это означает, что чем меньше требуется энергии на разрыв межатомных связей в молекуле данного соединения, тем больше его реакционная способность. [38]
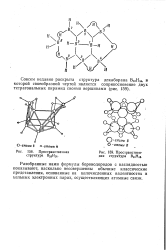 |
Пространственная структура ВюН1в. [39] |
Разобранные нами формулы бороводородов с наглядностью показывают, насколько несовершенны обычные классические представления, основанные на целочисленных валентностях и цельных электронных парах, осуществляющих атомные связи. [40]
Атомные связи часто приводят к образованию особо прочных комплексных соединений. Не только радикалы, но и нейтральные группы, например NH3, связываются атомными связями с центральным атомом особенно прочно. В отличие от них такие координационные соединения, в которых существуют только ионные связи - между сильно полярными молекулами и ионами ( без значительной доли гомеополярности), в большинстве случаев обладают только свойствами относительно слабых комплексных соединений. [41]
Атомные связи часто приводят к образованию особо прочных комплексных соединений. Не только радикалы, но и нейтральные группы, / например NH3, связываются атомными связями с центральным атомом особенно прочно. В отличие от них такие координационные соединения, в которых существуют только ионные связи между сильно полярными молекулами я ионами ( без значительной доли гомеополярности), в большинстве случаев обладают только свойствами относительно слабых комплексных соединений. [42]
Разрушение кристаллической решетки при плавлении металла еще не означает полного уничтожения упорядоченности в расположении атомов. Атомные связи при плавлении ослабляются сравнительно немного, и относительное размещение ближних атомов почти сохраняется. [43]
Атомные связи часто приводят к образованию особо прочных комплексных соединений. Не только радикалы, но и нейтральные группы, например NH3, связываются атомными связями с центральным атомом особенно прочно. В отличие от них такие координационные соединения, в которых существуют только ионные связи между сильно полярными молекулами и ионами ( без значительной доли гомеополярности), в большинстве случаев обладают только свойствами относительно слабых комплексных соединений. [44]
Пл Получаются непосредственно из элементов Энергии связи малы, поэтому соединения чаще всего неустойчивы. Все соединения имеют атомные связи. [45]
Страницы: 1 2 3 4