Донорно-акцепторные связи
Cтраница 1
Донорно-акцепторные связи могут образовываться между молекулами, в которых все атомы валентно насыщены и которые не содержат неспаренных электронов. Такие связи широко распространены в комплексных соединениях, кристаллогидратах солей и и др. Так, NHs, соединяясь с BF3, образует МНз BF3 благодаря наличию свободных орбит в атоме бора и неподеленных электронных пар в атоме азота. Прочность таких связей может достигать прочности обычных ковалентных связей. [1]
Донорно-акцепторные связи характерны для комплексных соединений, называемых также донорно-акцепторными комплексами. [2]
Донорно-акцепторные связи могут образовываться между молекулами, в которых все атомы валентно насыщены и которые не содержат неспаренных электронов. Такие связи широко распространены в комплексных соединениях, кристаллогидратах солей и др. Так, ННз, соединяясь с ВРз образует NHs - BF3 благодаря наличию свободных орбит в атоме бора и неподеленных электронных пар в атоме азота. Прочность таких связей может достигать прочности обычных ковалентных связей. При этом часто играет роль то, что из двух нейтральных частиц при образовании между ними донорно-акцепторной связи одна ( донор) становится заряженной положительно, а другая ( акцептор) - отрицательно, что приводит к электростатическому притяжению между ними. [3]
Донорно-акцепторные связи играют важнейшую роль при образовании комплексных соединений. [4]
Донорно-акцепторные связи, называемые также семиполярными, могут рассматриваться как результат наложения ковалентной и электровалентной связей; они обладают жесткостью, присущей ковалентной связи, однако образующие связь атомы несут электрический заряд, как в случае электровалентной связи. [5]
Донорно-акцепторные связи, как и ковалентные, по свойствам симметрии могут быть о - и л-типа. [6]
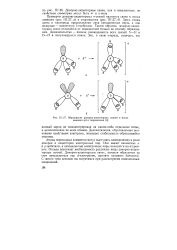 |
Образование донорно-акцепторных связей в ионах аммония ( а и гидроксония ( б. [7] |
Донорно-акцепторные связи, как и ковалентные, по свойствам симметрии могут быть ст - и я-типа. [8]
Донорно-акцепторные связи могут образовываться между молекулами, в которых все атомы валентно насыщены и которые не содержат неспаренных электронов. Такие связи широко распространены в комплексных соединениях, кристаллогидратах солей и и др. Так, МН3, соединяясь с BF3, образует NH3 BF3 благодаря наличию свободных орбит в атоме бора и неподеленных электронных пар в атоме азота. Прочность таких связей может достигать прочности обычных ковалентных связей. [9]
Донорно-акцепторные связи играют важнейшую роль при образовании комплексных соединений. [10]
Донорно-акцепторные связи могут образовываться между молекулами, в которых все атомы валентно-насыщены и которые не содержат неспаренных электронов. [11]
Донорно-акцепторные связи играют важнейшую роль при образовании комплексных соединений. [12]
Донорно-акцепторные связи часто сочетаются с ковалентными. Примером могут служить соединения типа - Si - О-Si -, в которых ковалентные связи Si-О усилены донорно-акцепторным взаимодействием. [13]
Часто донорно-акцепторные связи обозначают стрелкой, направление которой указывает направление смещения электронной пары. Если не акцентируется внимание на донорно-акцепторном характере связи, ее обозначают, как и ковалентную связь, черточкой. Иногда этим подчеркивают отсутствие принципиального различия между донорно-акцепторной и ковалентной связями. [14]
Донорно-акцепторные связи я-типа образуются только наряду с о-связями. Зачастую донором служит ион металла, представляющий в общее пользование свои спаренные d - электроны, а акцептором является лиганд, имеющий достаточно выгодные энергетические вакантные орбитали. [15]
Страницы: 1 2 3 4