Связывание - атом
Cтраница 3
Изменение основности происходит при введении СО, причем не только вследствие связывания атома азота, имеющего свободную пару электронов, с 5 /) 2-гибридизованным атомом углерода электроноакцепторной группы ( ср. [31]
В этом случае сначала определяют число ионов водорода, необходимое для связывания атомов кислорода в сложном ионе МпСУ, а затем уже находят число присоединяемых электронов. [32]
 |
Электронная структура ацетилена. [33] |
Из табл. 10 мы извлекаем еще одну, третью возможность для связывания атомов углерода. [34]
Перегруппировки молекулярные - превращение органического соединения, заключающееся в изменении последовательности связывания атомов в молекуле, кратности связей, положения кратных связей или совокупности этих изменеинй. [35]
Химическая структура аморфных алюмосиликатных катализаторов неоднородна, что обусловлено различной степенью связывания атомов алюминия с окисью кремния, а также наличием свободных окислов алюминия и кремния, не вошедших в алюмосиликат-ные комплексы. [36]
 |
Экспериментальная установка. [37] |
Доля излучения, которое испускается или поглощается без отдачи, зависит от связывания атома в кристалле, энергии у-лучей и температуры. В дальнейшем это свойство не будет использоваться, за исключением положения, что все опыты должны проводиться при температуре жидкого гелия, чтобы эффект был значительным. [38]
Сумма этих слагаемых должна учитывать все возможные комбинации, возникающие в результате попарного связывания атомов углерода за счет я-электронов. [39]
Сумма этих слагаемых должна учитывать все возможные комбинации, возникающие в результате попарного связывания атомов углерода за счет л-электронов. [40]
Льюиса, Лангмюра и Сиджвика, придающих важное значение электронным парам в связывании атомов между собой, развилось представление, что лигандами являются обязательно ионы или молекулы, которые содержат неподеленную пару электронов, как, например, в [: С1: ] - или H3N:, которая может быть использована для образования дативных ( донорных) связей, называемых также координационными связями с ионами металлов. [41]
В молекуле СО имеются две свободные пары электронов, не принимающие участия в связывании атомов С и О. Одна пара находится на нереакционной s - орбитали кислорода, а другая - на р-орбитали углерода, вытянутой в сторону, противоположную связи С-О. [42]
Изомерами называют соединения, имеющие одинаковый элементный состав, но различающиеся либо характером последовательности связывания атомов, либо их расположением в пространстве. [43]
Как видим, в каждом примере структурные изомеры имеют одинаковый состав, но различаются последовательностью связывания атомов в структурных формулах. [44]
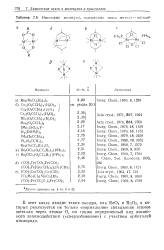 |
Некоторые молекулы, содержащие связи металл - металл3. [45] |
Страницы: 1 2 3 4