Связывание - металл
Cтраница 2
Варьируя условия эксперимента, можно изменять степень связывания металла в окрашенный комплекс, что в свою очередь позволяет соответственно изменять состав изучаемых бесцветных комплексов. [16]
Из вышеизложенного ясно, что идентификация центров связывания металла осуществляется наиболее просто в том случае, когда все они относятся к одному классу и ( или) когда они в точности совпадают со связывающим центром в известных модельных системах. Для идентификации уникальных центров связывания в данном конкретном белке, по-видимому, необходимы новые методы. Ясно, что даже полное представление о трехмерной структуре белка ( см. миоглобин) в настоящее время не дает возможности предсказать детально ни природу связывающих центров, ни влияние связывания на свойства белка. Для того чтобы делать какие-либо предсказания в этой области, необходимо получить более количественные представления о влиянии потенциальных лиганд-ных атомов на конформацию белка. [17]
После того как была обнаружена идентичность констант связывания металла с двумя центрами белка, тотчас же возник вопрос, идентичны ли сами связывающие центры. Эту проблему особенно трудно решить для белков, построенных из одной полипептидной цепи. И физиологические, и физические исследования пролили свет на эту еще не до конца решенную проблему, к которой мы ниже вернемся. [18]
При этом общее число электронов, участвующих в связывании металла с лигандами, уменьшается на два и атом металла претерпевает формальное восстановление. Этот процесс, а также обратная реакция играют важную роль в каталитическом гидрировании, изомеризации олефинов и гидроформ ил ировании. [19]
Часто сообщалось о том, что ГМФ эффективен в координационном связывании металлов. Его стерилизующее действие может быть объяснено этой его способностью, поскольку связывание важных, совместно действующих металлических компонентов может подавить любую из ферментных систем. [20]
В спектре первого появление полосы МН2 - группы указывает на связывание металла с азотом аминогруппы, в то время как частоты карбоксилатных групп ( 1588 и 1404 см -) такие же, как для свободной СОО - - группы. Существование и структура полиядерного иона [ Zn Zn ( Cys) 2 2 ] 2 во втором комплексе еще находятся под сомнением, но дублетная полоса ( 1510, 1600 см -) и сильно асимметричная полоса валентных колебаний карбоксилатной группы ( 1642 см -) интерпретируются как доказательство того, что МНз-группы цистеина свободны, а СОО - - груп-пы координированы. При отсутствии эффектов кристаллического поля такая координация соответствует ожидаемой. [21]
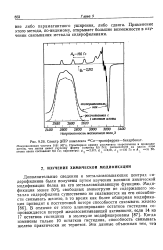 |
Спектр ЭПР комплекса 65Си - трансферрин-бикарбонат. [22] |
Применение этого метода, по-видимому, открывает большие возможности в изучении связывания металла сидерофилинами. [23]
Существуют некоторые разногласия по поводу значения чисел, полученных при измерении связывания металла с сидерофилинами методом равновесного диализа. [24]
Изучение взаимодействия между пептидами и Ni ( II) помогает получить представление о связывании металла пептидными атомами азота в комплексах Cu ( II) - пептид. Существование комплекса Ni ( II), в котором пептидные группы депротонированы, подтверждено препаративным [68], потенциометрическим 60, 69 - 71 ], ИК-спектроскопическим [60] и кристаллографическим [72] исследованиями; все они дают результаты, очень похожие на те, что получены для системы Си ( II) - пептиды. Термодинамическая устойчивость комплексов Ni ( II) - пептиды несколько ниже, чем устойчивость соответствующих Си ( II) - пептидных комплексов. [25]
Хотя длина связи медь - медь ( 4 4 А) слишком велика для связывания металлов, два атома электронно связаны через циклическую систему. [26]
Гибкость связей имидазол-металл может быть одной из причин эффективности гистидиновых боковых цепей как центров связывания металла в белках. Другой причиной может быть тот простой факт, что имидазольные группы являются достаточно хорошими донорами электронов для того, чтобы образовать сильные ковалентные связи. Изменения энтальпии, связанные с комплексообразованием ионов М2 в растворе с образованием [ M ( ImH) 4 ] 2, составляют - 23 0, - 18 4 и - 16 2 ккал / моль, когда M Cu, Ni и Zn соответственно. Наиболее важные вклады в энергик связей металл - имидазольный азот дает or - связывание. Возможно также я-связывание и влияние ЭСКП. Данные о d - р - связывании изменяются от комплекса к комплексу ( см. ниже), а когда ЭСКП вообще есть, она играет меньшую роль в стабилизации связей с имидазольным азотом, чем с атомами азота амино - и пептидных групп. [27]
Многообразие структур асфальтеновых молекул создает, очевидно, значительное число самых разнообразных возможностей для координационного связывания металлов. [28]
Инертная пара электронов в комплексах Sn ( II) в значительной мере уменьшает степень обратного двойного связывания металла. Несмотря на это, заполненные d - орбитали Sn ( II) обусловливают тот факт, что наиболее прочные комплексы образуются с поляризующимися лигандами, а отсутствие стабилизации полем лигандов ( поскольку олово является системой di0) приводит к тому, что нейтральные амины менее эффективны, чем анионы. [29]
Гидроксильные группы боковых цепей серина, треонина и тирозина, по-видимому, не являются местами связывания металла. Анализ кристаллической структуры № ( ь - 8ег) 2 ( ОН2) 2 [123], Cu ( L-Ser) 2 [124] и Zn ( L-Ser) 2 [125] подтверждает, что координация осуществляется только через атом азота аминогруппы и карбоксильный кислород. [30]
Страницы: 1 2 3 4