Связывание - противоион
Cтраница 2
Практический осмотический коэффициент рр не только не увеличивается с разбавлением, а даже иногда уменьшается, что противоречит характеру изменения свойств и ионных ассоциатов ( модель Раиса - Гарриса), и обычных низкомолекулярных сильных электролитов. Разбавление растворов полиэлектролитов сопровождается связыванием противоионов, что подтверждает большую роль электростатического поля, образованного цилиндрическим симметричным полимерным стержнем. [16]
Однако абсолютные значения а, вычисленные согласно этой тео рии, оказываются значительно выше экспериментальных. В известной мере это расхождение обусловлено тем, что не учитывается связывание противоионов. [17]
Пластинчатые мицеллы являют собой пример жидкокристаллического состояния вещества. Пластинчатые мицеллы, в отличие от сферических, слабо заряжены, что обусловлено высокой степенью связывания противоионов поверхностью мицелл вследствие высокой ионной силы концентрированных растворов ПАВ. [18]
Большие расхождения между теоретически предсказываемыми и экспериментально наблюдаемыми значениями степени вытягивания цепей свидетельствуют о несовершенстве теоретических расчетов, что отчасти объясняется пренебрежением связыванием противоионов, вызывающим снижение эффективной плотности заряда. Это допущение, по-видимому, неприемлемо, за исключением предельного случая использования растворителей с очень высокой ионной силой. В этом случае электростатические взаимодействия ближнего и дальнего порядка практически не имеют значения. Если принять, что различие между предсказываемым теоретически и экспериментально наблюдаемым ( по сравнению с размером в неионизованном состоянии) значениями степени вытягивания цепи обусловлено лишь экранирующим влиянием противо-понов, то таким путем можно оценить величину эффекта экранирования. Этот способ оценки приводит к выводу [76] о связывании примерно двух третей противоионов. [19]
 |
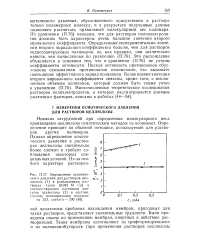
Зависимость между электрофоретической подвижностью яичного альбумина и количеством сильной кислоты или щелочи, которая пошла на его титрование. Ионная сила 0 01. рН изменялся от 3 1 до 11 7. [20] |
Из табл. 2 видно, что данные, полученные по мембранному потенциалу, очень хорошо совпадают с электрофоретическими, и совпадение улучшается с уменьшением ионной силы. Заряд белка, найденный титрованием, заметно отличается от полученного электрофорезом, несмотря на то что кривая титрования была сдвинута так, чтобы ее пересечение с осью абсцисс совпало с изоэлектрической точкой: заряд, найденный по подвижности, получается меньше, что несомненно следует приписать связыванию противоионов. [21]
В этом ряду по мере уменьшения ионного радиуса увеличивается гидратация ионов и, следовательно, их дегидратирующая способность. Кажущееся противоречие обусловлено тем, что образование гидратной оболочки экранирует заряд противоионов и снижает их способность связываться с поверхностью мицеллы. Между тем связывание противоионов приводит к уменьшению плотности поверхностного заряда мицелл и снижению электрических сил отталкивания, препятствующих мицеллообразованию. Действие этого фактора уменьшается в ряду от Cs к Li, и наблюдается снижение эффективности влияния противоионов на ККМ. [22]
Проведено исследование процесса эмульгирования в растворах электролитов и ПАВ. ПАВ и состава адсорбционного слоя Исследование процесса эмульгирования в бинарных растворах неионных и ионных ПАВ показало, что эффективность процесса больше в растворах, содержащих анионное ПАВ. Предложен метод оценки степени связывания противоионов для адсорбционных слоев, сформированных парами неионное-катионное и неионное-анионное ПАВ, основанный на измерении электрокинетического потенциала в зависимости от доли ионного компонента в адсорбционном слое. [23]
Из уравнения (11.76) находим, что для растворов полиэлектролитов должны быть характерны очень большие значения второго вириального коэффициента. Это расхождение объясняется в основном тем, что в уравнении (11.76) не учтены коэффициенты активности. Низкая активность противоионов обусловлена связыванием противоионов полиионами, что вызывает уменьшение эффективного заряда полиионов. [25]
Практический осмотический коэффициент срр не только не увеличивается с разбавлением, а даже иногда уменьшается, что. Разбавление растворов полиэлектролитов сопровождается связыванием противоионов, что подтверждает большую роль электростатического доля, образованного цилиндрическим симметричным полимерным стержнем. [26]
При не слишком малых ионных силах решение уравнения (1.149) дает а5 - М / з, как и для незаряженных макромолекул. Однако абсолютные значения а, вычисленные согласно этой тео-рии, оказываются значительно выше экспериментальных. В известной мере это расхождение обусловлено тем, что не учитывается связывание противоионов. [27]
Свойства мицедлярных электролитов не согласуются с моделью диффузионного двойного слоя противоионов между поверхностью мицеллы и объемом раствора. Наблюдаемый электрический потенциал на поверхности мицеллы невелик. Как эти факты, так и другие ( например, перенос Na к аноду в растворах амфифильных RCO Na) объясняются только гетероионной ассоциацией ионов мицеллы с противоионами ( о связывании противоионов см. разд. [28]
Они позволяют определить мицеллярную массу ( из совокупности данных по вязкости и диффузии, по ультрацентрифугированию и диффузии), оценить форму мицелл, рассчитать степень гидратации; 2) методы, основанные на изучении рассеяния света и рентгеновского излучения. Они дают сведения о размере и заряде мицелл ( светорассеяние), об их структуре ( дифракция рентгеновских лучей под малыми углами); 3) спектроскопические методы, среди которых наибольший объем информации о мицеллах ( структура мицелл, скорость обмена молекулами с мономерным ПАВ, состояние углеводородных радикалов в мицелле, состав смешанных мицелл и другие свойства) дает метод ядерного магнитного резонанса. При этом используется магнитный резонанс ядер Н, а также 19F и 13С; 4) электрохимические методы ( изучение электропроводности, электрофоретической подвижности, активности противоионов) позволяют получить данные об электрическом заряде мицелл, степени связывания противоионов мицеллой, электрокинетическом потенциале. [29]
Страницы: 1 2