Связь - кислород
Cтраница 1
Связь кислорода с углеродом не может быть чисто ковалентной или ионной. Судя по степени электроотрицательности углерода и кислорода, эта связь должна быть ионно-ковалентной со смещением отрицательного заряда в сторону кислорода. [1]
Связь кислорода с углеродом в комплексах CXHVOZ, по-видимому, аналогична хемосорбционной связи кислорода с углеродом в комплексах, образующихся при окислении твердого углерода. [2]
Связь кислорода с ароматическим атомом углерода обладает высокой прочностью из-за сопряжения орбитали НЭП кислорода с л-орбиталями кольца. Фенолы в отличие от спиртов не превращаются в арилгалогениды при нагревании с концентрированными галогеноводородными кислотами и при действии галогенидов серы и фосфора. [3]
Энергия связи кислорода на поверхности катализатора является, таким образом, одним из существенных факторов, определяющих активность окислов в отношении реакций окисления. Скорость же изотопного обмена в молекулярном кислороде, легко определяемая экспериментально, может служить удобной количественной характеристикой реакционной способности кислорода поверхности катализаторов. [4]
Энергия связи кислорода в оксиде железа ( Ш) значительно выше энергии связи для оксидов кобальта и никеля, значения которых близки. Установлено [104, 105], что при низких температурах регенерации процесс лимитируется отрывом кислорода от решетки оксида, и в уравнении, связывающем энергию активации процесса с энергией связи кислорода катализатора, Е Е0 щ, будет знак плюс. В этом случае снижение энергии связи кислорода должно уменьшать энергию активации процесса в целом и увеличивать скорость выгорания углерода. Следовательно, при 450 С наиболее медленно выгорание углерода протекает на оксиде железа ( Ш), так как кислород в данном случае связан наиболее прочно. [5]
Энергия связи кислорода с металлом ( на 1 моль связанного кислорода) будет максимальной при хемосорбции кислорода и постепенно уменьшается при образовании оксидов с более высокой степенью окисления, например, с утолщением хемосорбированного слоя и переходом его к барьерным и далее к фазовым слоям оксида. Создание структуры, характерной для образующегося фазового слоя на поверхности при энергичном окислительном воздействии, происходит также постепенно. Не всегда можно сделать вполне определенное заключение, о том, вызвана ли пассивность образованием мономолекулярного хемосорбционного слоя, присутствием более утолщенного барьерного слоя или образованием явного фазового слоя на внешней поверхности. [6]
Энергии связи кислорода в этих соединениях сравнимы с энергией связи исходной молекулы кислорода. [7]
Прочность связи кислорода с поверхностью платины возрастает с повышением потенциала анода, что приводит к увеличению энергии активации ра спада поверхностных кислородных соединений и повышению перенапряжения кислорода. При потенциалах выше 2 0 В состояние поверхности платины меняется вследствие появления; хемосорбированных кислородных соединений радикального характера, образующихся дри разряде соответствующих анионов. [8]
 |
Площадь растекания индия / и припоя ПСр 72 ( 2 по никелю марки НП-2 в зависимости от степени вакуумирования. Температура пайки 850 С, выдержка 5 мин.| Площадь растекания ( S и прочность. [9] |
Прочность связи кислорода с металлами увеличивается в направлении Ag-Cu-Ni - Fe, поэтому для оценки влияния на процесс растекания припоев устойчивости окиснои пленки на основном металле в качестве последнего было исследовано серебро. Окислы серебра в атмосфере воздуха разлагаются уже при 200 С. При более высоких температурах на поверхности серебра не будет окиснои пленки, исключается образование и слоя адсорбированного кислорода. Поэтому площадь растекания припоев в камере пайки, предварительно заполненной воздухом, не должна зависеть от степени вакуумирования. Эксперименты показали, что растекание индия и олова по серебру при 500 С не зависит от степени разрежения. [10]
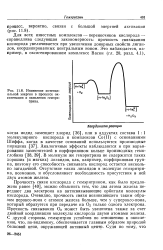 |
Изменение потенциальной энергии в процессе ок-сигенации и окисления гемэри-трина. [11] |
Прочность связи кислорода с гемэритрином, как было предложено ранее [40], можно объяснить тем, что два атома железа передают два электрона на антисвязывающие орбитали молекулы кислорода. Очевидно, прочность связи возникающего таким образом пероксо-иона с атомом железа больше, чем у супероксо-иона, который образуется при передаче на О2 только одного электрона. Прочность связывания О2 может быть увеличена также за счет двойной координации молекулы кислорода двумя атомами железа. С другой стороны, гемэритрин устойчив по отношению к окислению, что, по-видимому, обеспечивается главным образом природой белковой цепи, окружающей активный центр. [12]
Энергия связи кислорода в поверхностном слое окисных катализаторов в значительной степени определяет их каталитические свойства в отношении реакции окисления. Это обусловлено тем, что энергия связи кислорода с катализатором может в определенной доле входить слагаемым в величину энергии активации этих реакций. Удобной характеристикой прочности связи кислорода на поверхности окислов и его реакционной способности может служить скорость гомомолекулярного изотопного обмена кислорода. Нами предложено также определять энергию связи кислорода в поверхностном слое окисла из температурной зависимости равновесного давления кислорода над окислом при постоянном содержании кислорода в приповерхностном слое. Для этой цели разработана масс-спектрометрическая методика с применением омегатрон-ного измерителя парциальных давлений ИПДО. Найдена хорошая корреляция между энергиями активации реакций гомомолекулярного обмена кислорода, окисления метана и окисления водорода и энергиями связи кислорода на поверхности окислов металлов IV периода. Хорошая корреляция энергий связи кислорода и каталитической активности установлена и для бинарных окисных катализаторов шшгаельной структуры - кобальтитов и хромитов. [13]
Характер связи кислорода с поверхностью катализатора определяет скорость поверхностного окисления углеводородов и строение активных лабильных форм. Однако неспаренные электроны в молекуле кислорода не ослабляют, а упрочняют связь между атомами. [14]
Энергия связи кислорода катализатора, очевидно, имеет первостепенное значение для окисления нафталина. Инертность катализатора с К2С2Н2 ( СО2) 2 и А12О3, очевидно, объясняется тем, что сжигающее действие А12О3 [8] относится только к продуктам окисления. Калиевые катализаторы, имеющие несколько более высокую энергию связи кислорода, по сравнению с подобного состава натриевыми, содержат больше V5 и отличаются большей активностью. Селективность окисления нафталина зависит от энергии связи хемосорбированного кислорода. Натриевый катализатор с соотношением 1: 4: 5, имеющий энергию связи кислорода, близкую к калиевому с соотношением 1: 2: 8, и слабую интенсивность десорбции О2 ( см. табл. 2), отличается большей избирательностью по продуктам сгорания. Несколько выпадает из этой закономерности образец с Li. Это, возможно, связано с тем, что литий значительно отличается по химическим свойствам от других щелочных металлов. [15]
Страницы: 1 2 3 4