Связь - кислород
Cтраница 3
Для характеристики прочности связи кислорода с поверхностью оксидного катализатора в разное время использовали различные величины: давление диссоциации оксидов при фазовых переходах, энтальпию образования оксидов из элементов, отнесенную к 1 моль кислорода, теплоту превращения низших оксидов в высшие, теплоту сорбции кислорода, восстанавливаемость оксидов, энергию активации изотопного обмена кислорода, скорость гомомолекулярного обмена кирло-рода и др. Из указанных величин первые три, связанные с фа-з овыми переходами оксидов, выбрали, исходя из представлений о том, что каталитическая реакция окисления в качестве промежуточных стадий включает переходы оксидов из одного фазового состояния в другое с различными валентными состояниями катионов. Сопоставление активностей оксидных катализаторов в реакциях глубокого окисления различных веществ со скоростями гомомолекулярного изотопного обмена кислорода на этих катализаторах выявляет достаточно четкие корреляции, однако некоторые оксиды ( например, оксид ванадия и оксид титана) выпадают из общей закономерности. [31]
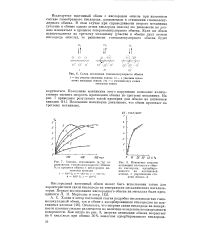 |
Схема механизма гомомолекулярного обмена.| Изменение энергии активации изотопного обмена кислорода, адсорбированного на платиновой пленке, с увеличением степени обмена X. [32] |
Оказалось, что энергия связи кислорода на поверхности платины сильно различается по величине вследствие неоднородности поверхности. Как видно из рис. 8, энергия активации обмена возрастает на 6 ккал / молъ при обмене 30 % монослоя адсорбированного кислорода. [33]
В качестве меры прочности связи кислорода в исследованных солях нами использованы величины энергии активации процесса изотопного обмена и удельный обмен - степень обмена ( в %), достигнутая при определенной температуре за известный промежуток времени, отнесенная к 1 м2 поверхности соли. В табл. 3 представлены соответствующие цифры. [34]
 |
Схема перехода полярной структуры в ионную. [35] |
В молекулах оснований из связей кислорода - с металлом и водородом - легче ионизируется первая. Таким образом, основания можно определить как соединения, дающие в водном растворе ионы гидроксила. [36]
Проанализированы взаимоотношения между прочностью связи кислорода ( 7s) с поверхностью металлов и окислов и их каталитической активностью в отношении окисления водорода, окиси углерода, аммиака и сернистого газа. Во всех случаях ( за исключением окисления SO2 на окислах) зависимость каталитической активности от qs выражается характерными кривыми с максимумом, положение которого определяется принципом энергетического соответствия. При окислении сернистого газа на окислах значение qs для наиболее активного катализатора ( V2O5) существенно отличается от ( qs) опт, рассчитанного теоретически. Это объясняется тем, что VjOs не является истинным оптимальным катализатором данной реакции; окислы, qs для которых близко к ( fs) oni ( СозО4, MnC2, NiO), неустойчивы в условиях сернокислотного катализа. Проведено также сопоставление термодинамических свойств веществ и их каталитической активности в отношении окисления хлористого водорода. [37]
Проанализированы взаимоотношения между прочностью связи кислорода с поверхностью металлов и окислов ( qs) и их каталитической активностью в отношении полного окисления парафинов, циклопарафинов, олефинов, ацетиленовых и ароматических углеводородов, метанола и некоторых других веществ. [38]
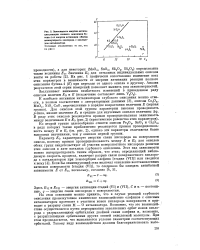 |
Зависимость энергии активации реакции полного окисления бу-тена-1 от энергии активации обмена молекулярного кислорода с кислородом катализатора. [39] |
Параметр EQ характеризует энергию связи кислорода на поверхности окисла, поэтому прямая пропорциональность между Е и EQ для окислов обеих групп свидетельствует об участии поверхностного кислорода решетки этих окислов в акте катализа глубокого окисления. [40]
Таким образом, энергия связи кислорода на поверхности катализатора является одним из существенных факторов, определяющих активность окислов в реакциях окисления. [41]
В молекулах оснований из связей кислорода с металлом а водородом легче ионизируется первая. Таким обра зом, основания можно определить как соединения, дающие в водном растворе ионы гидроксила. [42]
Таким образом, характер связи кислорода и углеводорода на поверхности платины иной, чем на серебре. Вследствие большой прочности связей адсорбированного кислорода и углеводорода реакция образования окиси этилена на платине маловероятна. Кроме того, на платине даже при 70 обнаружено объемное продолжение реакции окисления пропилена. [43]
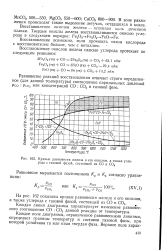 |
Кривые равновесия железа и его окислов, а также углерода с газовой фазой, состоящей из СО и СО3. [44] |
Восстановление возможно, если прочность связи кислорода с восстановителем больше, чем с металлом. [45]
Страницы: 1 2 3 4