Связь - кольцо
Cтраница 3
Многочисленные исследования Б. А. Казанского и его сотрудников показали, что только платина является таким специфическим катализатором, ускоряющим гидрогенолиз С-С - связей пентаметиленового кольца и пассивным по отношению к гидрогенолизу обычных парафиновых углерод-углеродных связей. [31]
 |
Цитидин. Цепи водородных связей.| Цитидин. Проекция ab. [32] |
Центральная связь N3 - Cr расположена в плоскости пиримидинового кольца и образует тетраэдрические углы ( 109 и 115) с прилежащими связями кольца рибозы. Оба кольца молекулы почти перпендикулярны друг к другу. Связь С2 О2 чисто двойная, связь N3 - Q чисто одинарная, связь Ce - Ne сокращена, как и в ряде других производных пиримидина ( стр. [33]
У 4-диметилсульфилимино - З - фенилфуроксана, в котором на атоме азота заместителя имеется избыточный отрицательный заряд, тенденция к удлинению примыкающих связей кольца усиливается. Все три связи кольца С-С, С N и N-О в этом соединении самые длинные среди всех до сих пор изученных рентгенографически фуроксановых соединений. [34]
У 4-диметнлсульфнлнмнно - З - фенилфуроксана, в котором на атоме азота заместителя имеется избыточный отрицательный заряд, тенденция к удлинению примыкающих связей кольца усиливается. Все три связи кольца С-С, С N и N-О в этом соединении самые длинные среди асех до сих пор изученных рентгенографически фуроксановых соединений. [35]
В ходе этих исследований было замечено, что скорости гидрогенолиза изученных углеводородов сильно зависят от строения молекулы, уменьшаясь с увеличением числа связей кольца, экранированных метильными группами. [36]
Возможно, избирательный гидрогенолиз одной связи С-С циклопентана связан с дублетно-секстетной реакцией, в та время как дублетная реакция приводит к беспорядочному разрыву связей кольца циклопентана. Таким образом, различный характер адсорбции циклопентана, который проявляется в изменении вида кривой распределения при дейтерообмене, приводит, очевидно, и к разному протеканию реакции. В то же время для Pt и Pd характер адсорбции циклоалканов, насколько можяо судить по виду кривой распределения дейтероалканов, а также структурные особенности кристаллической решетки и энергия связи с циклопента-ном [220] весьма близки, а резко различная каталитическая активность этих двух металлов в реакциях гидрогенолиза циклопентана может быть связана с какими-то иными их свойствами, например с различной растворимостью в них водорода. [37]
Можно предположить, что поразительная прочность связи ди-иминоизоиндолинового лиганда в комплексе объясняется образованием водородных мостиков между иминогруппами лиганда и двумя - С Ы - связями дегидрофталоцианинового кольца. [38]
Образование сильной короткой водородной связи в рассмотренных выше системах объясняется, по Шигорину [34, 35], участием внутримолекулярной водородной связи в передаче л-вза-имодействия по всей системе связей кольца. [39]
У циклических соединений свободное вращение вокруг углерод-углеродных связей отсутствует, поэтому цис-гранс-изомеры не могут легко переходить один в другой, это возможно лишь при разрыве связей кольца. [40]
На основании образования ферроцена при реакции C5H5Ti ( OG2H5) 3 и ( C5H5) 2Ti ( OCOCH3) 2 с FeCl2 и легкости гидролиза связи циклопентадие-нильного кольца с металлом в этих соединениях нами [1] было высказано предположение, что связь атома титана с циклопентадиенильными кольцами в CBH5Ti ( OC2H5) 3 и ( G8H5) 2Ti ( OCOCH3) 2 носит в значительной степени ионный характер. С другой стороны, нами было показано [1], что после замены в молекуле C5H5Ti ( OC2H8) 3 двух или даже одной этоксильной группы на атомы хлора взаимодействие с FeCl2 уже не приводит к образованию ферроцена. [41]
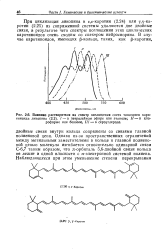 |
Влияние растворителя на спектр поглощения света типичного каро-тииоида ликопииа. / - в петролейиом эфире или этаноле. / / - в хлороформе или бензоле, / / / - в сероуглероде. [42] |
Однако из-за пространственных ограничений между метильными заместителями в кольце и главной полиеновой цепью молекула изгибается относительно одинарной связи С-67 таким образом, что я-орбиталь 5 6-двойной связи кольца не лежит в одной плоскости с я-электронной системой полиена. [43]
Такая фрагментация алкокси-радикалов появляется прежде всего тогда, когда кроме бедного энергией карбонильного соединения образуется низкоэнергетический радикал или может быть устранено напряжение кольца благодаря разрыву одной из связей кольца. [44]
Таким образом, приведенные данные показывают определенное сходство во влиянии алкильного заместителя, в частности метильной группы, на легкость разрыва и энергию активации гидрогенолиза С-С - связей кольца в углеводородах ряда циклогептана и циклопентана. [45]
Страницы: 1 2 3 4