Экспериментальное значение - константа
Cтраница 1
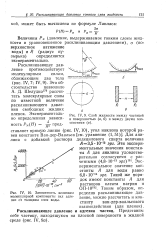 |
Слой жидкости между частицей.| Зависимость величины молекулярной компоненты сил адге. [1] |
Экспериментальное значение константы А для воды равно 6 0 10 - 14 эрг. [2]
Экспериментальные значения константы соответствуют из меренным значениям астр для потока с искусственной турбули-зацией, что, как было показано ранее, и имеет место при течении газа через шаровые укладки. [3]
Экспериментальные значения константы А значительно меньше теоретического и сильно отличаются для разных металлов. Температурный ход тока насыщения формула (61.1) передает вполне удовлетворительно. [4]
Экспериментальные значения констант могут быть определены так же, как и в случае зависимости температурного коэффициента приведения ат только от температуры. [5]
Экспериментальные значения констант скорости роста, полученные в подобных системах из кинетики полимеризации, являются поэтому сложными величинами. Такие суммарные константы / с2, включающие диссоциацию и рост ( V-48, 49), могут быть измерены при использовании для возбуждения полимеризации низкомолекулярных живых полимеров ( со степенью полимеризации от 10 до 20), что позволяет исключить стадию инициирования. Энергия активации, рассчитанная из температурного хода кинетики, имеет в различных системах бутиллитий-мономер-углеводород необычайно высокие значения ( 15 - 20 ккал. [6]
Экспериментальные значения констант скорости роста, полученные в подобных системах из кинетики полимеризации, являются поэтому сложными величинами. Такие суммарные константы / с2, включающие диссоциацию и рост ( V-48, 49), могут быть измерены при использовании для возбуждения полимеризации низкомолекулярных живых полимеров ( со степенью полимеризации от 10 до 20), что позволяет исключить стадию инициирования. Энергия активации, рассчитанная из температурного хода кинетики, имеет в различных системах бутиллитий-мономер-углеводород необычайно высокие значения ( 15 - 20 ккал. Причина этого состоит в том. [7]
 |
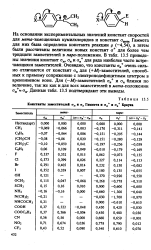
Константы заместителей ам и о Гаммета и ом и о Брауна. [8] |
На основании экспериментальных значений констант скоростей для мета-замещенных кумилхлоридов и констант ст Гаммета для них была определена константа реакции р ( - 4 54), а затем были рассчитаны величины новых констант ст для более чем тридцати заместителей в пора-положении. В табл. 13.5 приведены значения констант ам, ап и ап для ряда наиболее часто встречающихся заместителей. Очевидно, что константы стп очень сильно отличаются от констант стп для ( - Л /) - заместителей, способных к прямому сопряжению с электронодефицитным центром в аренониевом ионе. Для ( - Л /) - заместителей стп и ст близки по величине, так же как и для всех заместителей в жета-положении стм стм. Данные табл. 13.5 подтверждают эти выводы. [9]
На основе экспериментальных значений константы равновесия для реакции восстановления и данных рис. 10 определялась свободная энергия образования Nb3Sn, которая составляет от - 2 4 до - 5 1 ккал / моль. Эта величина вполне достоверна, поскольку олово и ниобий легко реагируют при 950 С. [10]
 |
Константы заместителей ам я а, Гаммета вм т, Брауна. [11] |
На основании экспериментальных значений констант скоростей для лета-замещенных кумилхлоридов и констант амета Гаммета для них была определена константа реакции р ( - 4 54), а затем были рассчитаны величины новых констант а для более чем тридцати заместителей в пора-положении. В табл. 13.5 приведены значения констант ам, а и ал для ряда наиболее часто встречающихся заместителей. Очевидно, что константы а очень сильно отличаются от констант а для ( Л) - заместителей, способных к прямому сопряжению с электронодефицитным центром в аренониевом ионе. Данные табл. 13.5 подтверждают эти выводы. [12]
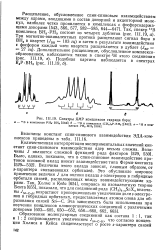 |
Спектры ЯМР комплексов гидрида бора. [13] |
Количественная интерпретация экспериментальных значений констант спин-спинового взаимодействия ядер весьма сложна. Величина этого вклада зависит, главным образом, от s - характера связывающих орбиталей. Это обусловило широкое применение величин / для оценки вклада s - электронов в гибридные орбитали связей, расположенных между взаимодействующими ядрами. Так, Холмс и Кейс [654], опираясь на изовалентную теорию Бента [655], показали, что для соединений ряда ( СН3) 4 5пХ величины / 5п он возрастают пропорционально увеличению доли s - электронов в гибридных орбиталях, предоставляемых атомом олова для образования связей Snf-С. [14]
При интерпретации экспериментальных значений констант скоростей термического распада молекул или времени жизни колебательно-возбужденных ионов часто приходилось рассматривать s как эмпирический параметр, интерпретируемый как число эффективно участвующих во внутримолекулярном обмене энергии гармонических осцилляторов [7], причем оказывалось, что 5эфф составляет лишь некоторую долю от общего числа колебательных степеней свободы. Такое толкование приводит к весьма неопределенной физической картине обмена энергии, поскольку приходится предполагать, что связь некоторых осцилляторов с координатой реакции, отличная от нуля в принципе даже в гармоническом приближении, должна быть меньше ангармонической связи между активными осцилляторами, которая обеспечивает статистический характер распределения энергии между ними. ЭФФ связано с некорректным применением классической теории для интерпретации экспериментов, для которых условие применимости этой теории ( Hii kT - для термического распада и Е - Ео 5& JIMS - для распада ионов в масс-спектрометрических условиях) не выполняется. Оставаясь последовательно в рамках модели Касселя, невозможно выделить определенные колебательно-возбужденные конфигурации, которые можно было бы исключить из рассмотрения внутримолекулярного обмена энергии, поскольку такое исключение противоречило бы самой сущности модели. Однако если активированное состояние обладает определенной симметрией, то полные волновые функции колебательно-возбужденной молекулы, учитывающие ангармоническую связь между осцилляторами, но отвечающие различным типам симметрии, не могут смешаться в результате внутримолекулярных взаимодействий. Формально этот эффект может проявиться как уменьшение эффективного числа степеней свободы по сравнению с истинным. [15]
Страницы: 1 2 3 4 5