Межмолекулярная водородная связь
Cтраница 2
Межмолекулярная водородная связь возникает между молекулами, в состав которых входят водород и сильно электроотрицательный элемент. [16]
Межмолекулярная водородная связь возникает между молекулами, в состав которых входят водород и сильно электроотрицательный элемент - фтор, кислород, азот, реже хлор, сера. Поскольку в такой молекуле общая электронная пара сильно смещена от водорода к атому электроотрицательного элемента, а положительный заряд водорода сконцентрирован в малом объеме, то протон взаимодействует с неподеленной электронной парой другого атома или иона, обобществляя ее. В результате образуется вторая, более слабая связь, получившая название водородной. [17]
Межмолекулярная водородная связь возникает между молекулами, в состав которых входят водород: л сильно электроотрицательный элемент - фтор, кислород, влот, реже хлор, сера. Поскольку в такой молекуле общая электронная пара сильно смещена от водорода к атому электроотрицательного элемента, л положительный заряд водорода сконцентрирован в малом объеме, то протон взаимодействует с неподеленной электронной парой другого атома или иона, обобществляя ее. В результате образуется вторая, более слабая связь, получившая название водородной. [18]
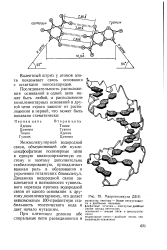 |
Макромолекула ДНК. [19] |
Межмолекулярной водородной связи, объединяющей обе нукле-озидфосфатные полимерные цепи в единую квазисопряженную систему и поэтому дополнительно стабилизированную, принадлежит важная роль в образовании и упрочении гигантских биомолекул. [20]
Влияние межмолекулярных водородных связей на свойства полиамидов опять-таки четко демонстрируется разницей в свойствах полигексаметиленсебацинамида ( найлон-610) и того же полиамида, у которого 60 % атомов водорода амидных групп замещены на алкильные группы. [21]
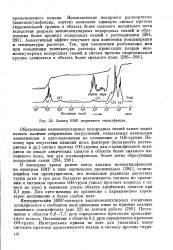 |
Спектр ЯМР вторичного гептилфенола. [22] |
Образованию межмолекулярных водородных связей также может мешать наличие стерйческих затруднений, создаваемых алкильным заместителем в орто-положении по отношению к ОН-группе. [23]
Образование межмолекулярной водородной связи в конденсированной фазе определяет различие в кислотности первичных, вторичных и третичных спиртов в газовой и конденсированной фазах. В газовой фазе кислотность спиртов уменьшается в ряду ( гл. [24]
Исследования межмолекулярной водородной связи связаны с определенными экспериментальными трудностями. Полосы часто оказываются широкими и слабыми; значительно влияние изменения фазового состояния и температуры; во многих случаях необходимы дополнительные исследования спектров комбинационного рассеяния. Можно считать, что в спектрах комплексов значения частот приближенно описывают потенциальную функцию равновесной конфигурации, а величины интенсивностей дают представление о миграции заряда при отклонении от равновесного состояния. Поскольку водородная связь играет важную роль в биологически активных молекулах, исследования в дальней инфракрасной области представляют исключительный интерес. В частности, низкочастотные колебания вносят большой вклад в энтропию водородной связи; они также необходимы в расчетах констант равновесия. Более подробное обсуждение этого вопроса проведено в гл. [25]
Множество межмолекулярных водородных связей, в том числе и просто между группами ОН, объединяет цепи целлюлозы в своеобразные пучки, из которых и возникают прочные волокна. Растворять целлюлозу могут лишь растворители, способствующие разрушению водородных связей. [26]
Образование межмолекулярных водородных связей между спиртами и водой является причиной того, что метанол, этанол, пропанол-1, пропанол-2 и 2-метилпропанол - 2 смешиваются с водой во всех отношениях. [27]
Образование межмолекулярных водородных связей сопряжено с частичным смещением протона от одной молекулы к другой. Это смещение, например при соединениях кислот с аминами, может варьировать в широком диапазоне - от связей ковалентных до связей ионных. [28]
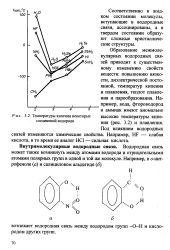 |
Температуры кипения некоторых соединений водорода. [29] |
Образование межмолекулярных водородных связей приводит к существенному изменению свойств веществ: повышению вязкости, диэлектрической постоянной, температур кипения и плавления, теплот плавления и парообразования. Например, вода, фтороводород и аммиак имеют аномально высокие температуры кипения ( рис. 3.2) и плавления. [30]
Страницы: 1 2 3 4