Двухэлектронная связь
Cтраница 2
Разрыв двухэлектронной связи А - В в зависимости от ее полярности и условий протекания процесса может быть двух типов. [16]
Формирование двухэлектронных связей ( ковалентные связи) происходит при образовании молекулы водорода и взаимодействии водорода с неметаллами. [17]
Формирование двухэлектронных связей ( ковалент-ные связи) происходит при образовании молекулы водорода и взаимодействии водорода с неметаллами. [18]
Разрыв двухэлектронной связи может сопровождаться переходом электронов на атомные орбиты разных атомов. В этом случае принято говорить, что происходит разрыв электронной пары, образующей связь. [19]
 |
Адсорбция на ионном кристалле. [20] |
Образование двухэлектронной связи и появление электрона на локальном уровне в запрещенной зоне может осуществляться двумя путями. Локализация электрона сопровождается выпадением его из зоны проводимости. Однако не исключена возможность появления электрона на локальном уровне за счет перехода его на этот уровень из валентной зоны, чему должно соответствовать возникновение свободной дырки в валентной зоне. [21]
Разрыв двухэлектронной связи может сопровождаться переходом электронов на атомные орбиты разных атомов. В этом случае: принято говорить, что происходит разрыв электронной пары, образующей связь. [22]
Разрыв двухэлектронной связи может, однако, идти и другим путем - без разрыва электронной пары, а именно: путем перехода обоих электронов на атомную орбиту одного из атомов. [23]
Образование двухэлектронной связи сопровождается заряжением поверхности отрицательным зарядом. Последний компенсируется положительным зарядом ионизованных доноров в объеме / Если атом А захватывает свободную дырку, он теряет свой валентный электрон и превращается в положительный ион. [24]
Такую двухэлектронную связь, в которой принимает участие электрон решетки, заимствованный из семейства свободных электронов, мы называем прочной гомеополярной связью. Заметим, что в состоянии прочной гомеополярной связи валентность атома А насыщена; она насыщена свободной валентностью поверхности. [25]
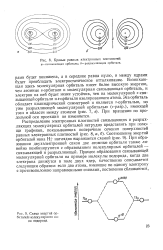 |
Кривые равных электронных плотностей. а-связывающая орбиталь. б-разрыхляющая орбиталь. [26] |
При образовании двухэлектронной связи две атомные орбитали также линейно комбинируются с образованием молекулярных орбиталей - связывающей и разрыхляющей. [27]
 |
Валентные состояния углерода. [28] |
При образовании двухэлектронной связи две атомные орбитали также линейно комбинируются с образованием молекулярных орбиталей - связывающей и разрыхляющей. Процесс образования связывающей молекулярной орбитали на примере молекулы водорода, когда два электрона движутся в поле двух ядер, качественно описывается следующим образом: если два атома, имеющие по одному электрону с противоположно направленными спинами, постепенно сближаются, то между ними начинают действовать силы притяжения; на близком же расстоянии возникают силы отталкивания, которые быстро возрастают. [29]
Поляризация одной двухэлектронной связи в сложной молекуле влияет на состояние соседних связей. Дипольный момент индуцирует в них также дипольные моменты, правда, значительно меньшие. Этот индуктивный эффект ( / - эффект) оказывает влияние на реакционную способность молекулы и особенно наглядно проявляется при сравнении констант диссоциации замещенных кислот. [30]
Страницы: 1 2 3 4