Двухцентровая двухэлектронная связь
Cтраница 1
Двухцентровая двухэлектронная связь в схемах изображается короткой линейной. В целом электронная структура молекулы выглядит как набор различных валентных схем, откуда вытекает второе название метода - метод локализованных пар. [1]
 |
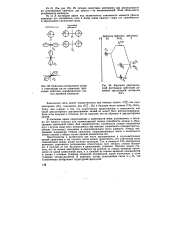
Взаимодействие атомов водорода ( а, атомов водорода с атомом азота ( б и валентная схема молекулы МН3 ( в. [2] |
Каждая двухцентровая двухэлектронная связь изображается валентным штрихом. Электронное состояние молекулы описывается с помощью валентных схем, откуда метод и получил свои названия - метод валентных схем, метод локализованных пар, метод валентных связей. [3]
Представление о валентности как числе двухцентровых и двухэлектронных связей применимо в тех случаях, когда можно представить, что химическая связь локализована между двумя атомами молекулы. Так, в молекуле СН4 электронная плотность равномерно распределена относительно всех четырех атомов водорода, и каждый из них находится в равноценных условиях. [5]
Представление о валентности как о числе двухцентровых и двухэлектронных связей применимо в тех случаях, когда можно представить, что химическая связь локализована между двумя атомами молекулы. [6]
 |
Перекрывание атомных орбиталей. [7] |
Четыре концевых атома водорода связаны с атомами бора обычными двухцентровыми двухэлектронными связями. Таким образом, из двенадцати валентных электронов, имеющихся в атомах, составляющих молекулу диборана, восемь участвуют в образовании двухцентровых связей В - Н, а четыре образут две трехцентровые связи В - Н - В. [8]
 |
Перэкрывание атомных орбиталей в молекуле диборана. [9] |
Четыре концевых атома водорода связаны с атомами бора обычными двухцентровыми двухэлектронными связями. Таким образом, из двенадцати валентных электронов, имеющихся в атомах, составляющих молекулу диборана, восемь участвуют в образовании двухцентровых связей В - Н, а четыре образуют две трехцентровые связи В - Н - В. [10]
 |
Перекрывание атомных орбиталей н. [11] |
Четыре концевых атома водорода связаны с атомами бора обычными двухцентровыми двухэлектронными связями. Таким образом, из двенадцати валентных электронов, имеющихся в атом ах, составляющих молекулу диборана, восемь участвуют в образовании двухцентровых связей В - Н, а четыре образут две трехцентровые связи В - Н - В. [12]
Четыре концевых атома водорода вязаны с атомами бора обычными двухцентровыми двухэлектронными связями. Таким образом, из двенадцати валентных электронов, имеющихся в атомах, составляющих молекулу диборана, восемь участвуют в образовании двухцеитровых связей В - Н, а четыре образут две трехцентровые связи В - Н - В. [13]
 |
Перекрывание атомных орбиталей в молекуле диборана. [14] |
Четыре концевых атома водорода связаны с атомами бора обычными двухцентровыми двухэлектронными связями. Таким образом, из двенадцати валентных электронов, имеющихся в атомах, со ставляющих молекулу диборана, восемь участвуют в образовании двухцентровы связей В - Н, а четыре образут две трехцентровые связи В - Н - В. [15]
Страницы: 1 2 3