Межмолекулярная связь
Cтраница 1
Межмолекулярная связь может иметь локальный или объемный характер. [1]
Межмолекулярная связь в этих комплексах возникает, вероятно, вследствие взаимодействия Зр2 - неподеленной пары электронов атома серы, с одной стороны, и вакантной орбиты молекулы йода, с другой. Следует ожидать, что образующиеся в результате донорно-акцепторного взаимодействия комплексные соединения должны иметь большие дипольные моменты. В этом случае метод диэлектрической поляризации является весьма эффективным для обнаружения и изучения комплексов. [2]
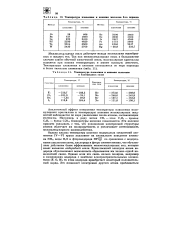 |
Температура плавления и кипения галогенов и благородных газов. [3] |
Межмолекулярная связь действует между молекулами газообразных и жидких тел. Так как межмолекулярная связь в большинстве случаев слабее обычной химической связи, молекулярные кристаллы плавятся при низких температурах и имеют высокую летучесть. [4]
 |
Структура молекулярных кристаллов брома, иода. Центры моле кул ( Вг, 1г совпадают с узлами ромбической гранедентрированной решетки. [5] |
Межмолекулярная связь 1 является наиболее общим видом связи. Впервые она была введена Ван-дер - Ваальсом ( 1873 г.) для объяснения отступления реальных газов от уравнения состояния идеальных газов. Отсюда происходит ее название. [6]
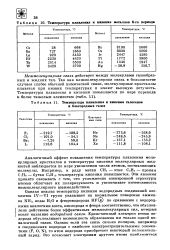 |
Температура плавления и кипения галогенов и благородных газов. [7] |
Межмолекулярная связь действует между молекулами газообразных и жидких тел. Так как межмолекулярная связь в большинстве случаев слабее обычной химической связи, молекулярные кристаллы плавятся при низких температурах и имеют высокую летучесть. [8]
Межмолекулярная связь в этих комплексах возникает, вероятно, вследствие взаимодействия 3 ] э2 - неподеленной пары электронов атома серы, с одной стороны, и вакантной орбиты молекулы йода, с другой. Следует ожидать, что образующиеся в результате донорно-акцепторного взаимодействия комплексные соединения должны иметь большие динольные моменты. В этом случае метод диэлектрической поляризации является весьма эффективным для обнаружения и изучения комплексов. [9]
Межмолекулярная связь может возникнуть за счет ориентационного, индукционного и дисперсионного взаимодействий, которые имеют электромагнитную природу. [10]
Межмолекулярная связь и химическая связь, осуществляемые за счет донорно-акцепторяых процессов, имеют общность, которая заключается в их электрической природе. В то же время между ними есть существенное различие. Для межмолекулярной связи характерно отсутствие перекрывания электронных облаков молекул. Эта связь проявляется еще до непосрественного контакта двух тел. Химическая связь за счет донорно-акцепторных процессов образуется парой электронов, принадлежащих адгезиву и субстрату, и проявляется только после их контакта. В результате реакции между адгезивом и субстратом могут возникнуть ионная и ковалентная связи, которые подобно донорно-акцепторной связи являются разновидностью химической связи. [11]
Межмолекулярная связь ( силы Ван-дер - Ваальса) характеризуется силой притяжения молекул в веществе между собой. [12]
Межмолекулярная связь, осуществляемая гидроксильным водородом, обозначена на схеме пунктиром. Как видно из схемы, таких связей две. В муравьиной кислоте на одну связь приходится энергия диссоциации 7 05 ккал / моль. Длина водородной связи равняется приблизительно 1 7 А. [13]
 |
Происхождение поверхностной энергии ( схема. [14] |
Возникает межмолекулярная связь: адсорбируемое вещество ( адсорбтив) - адсорбент. [15]
Страницы: 1 2 3 4 5