Межмолекулярная связь
Cтраница 2
Обычна межмолекулярная связь карбоксильных групп с другими основными группами. Значения константы равновесия и изменения энтальпии [238] при димеризации кислот в растворе бензола значительно меньше вследствие конкуренции цикла. В диок-сане кислоты мономерны по крайней мере в том смысле, что все молекулы кислоты связаны с растворителем и ни одна из них не связана с другой молекулой кислоты. Полученные результаты очень интересны, хотя полное объяснение им еще не дано. [16]
Энергия межмолекулярных связей и гибкость макромолекулы характеризуют подвижность молекулярных звеньев и структуры волокна в целом. [17]
Природа межмолекулярных связей ( их не принято называть химическими) также электрическая, однако эти связи значительно менее прочны ( в 10 - 100 раз), чем межатомные. [18]
Образование межмолекулярных связей в гибких аморфных полимерах вызывает увеличение прочности, начального модуля, расширение области высокоэластического состояния, снижение растворимости и в ряде случаев приводит к повышению теплостойкости. При структурировании аморфных жестких полимеров механические свойства изменяются в гораздо меньшей степени. [19]
 |
Наиболее плотные упаковки шаров одинакового диаметра. а - гранецентрированная. б - гексагональная. [20] |
Энергия межмолекулярных связей обычно невелика и кристаллы с такими связями ( например, GeCl4, GeI4, SiClJ имеют низкие температуры плавления и кипения. [21]
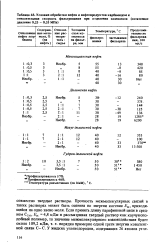 |
Условия обработки нефти и нефтепродуктов карбамидом и относительная скорость фильтрования при отделении комплекса ( остаточное давление 0 25 - 0 35 МПа. [22] |
Прочность межмолекулярных связей в таких растворах может быть оценена по энергии когезии Ек, приходящейся на одно звено моля. [23]
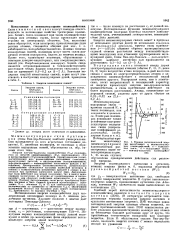 |
Энергия межатомных связей.| Кривые потенциальной энергии межатомных и межмолекулярных взаимодействий. а - ковалент-ная свячь, б - водородная связь, в - ван-дер-ваальсово взаимодействие. [24] |
Энергия межмолекулярных связей лежит в пределах от нескольких десятых долей до нескольких ккал / моль ( 1 ккал / лоль 4 2 кдж / молъ), причем силы притяжения / - ( dU / dr) убывают обратно пропорционально седьмой степени расстояния между взаимодействующими молекулами или атомными группировками молекулярной цепи. [25]
Наличие межмолекулярных связей способствует также большей кристалличности и меньшей растворимости полимера. [26]
Замена межмолекулярных связей валентными обусловливает нерастворимость и неплавкость смол, значительно увеличивает их прочность ( от 10 до 100 раз) и затрудняет процессы пластической деформации. К этим смолам относятся все термореактивные смолы в стадии С ( стр. [27]
Особенности межмолекулярных связей в коллагене зависят от вида и возраста организма, из которого он выделен. Важным компонентом структуры коллагена является вода. Расположение молекул воды в структуре коллагена точно еще не установлено. Рассмотренные выше модели позволяют интерпретировать лишь те рентгенографические данные, которые касаются - сравнительно небольших периодов - яне объясняют периода 640А, который виден в электронном микроскопе и на рентгенограммах, полученных под малыми углами. [28]
Природа межмолекулярных связей состоит в электростатическом взаимодействии, причем, в отличие от ионной и ковалентной связей, сдвиг электронов взаимодействующих молекул осуществляется внутри молекулы. [29]
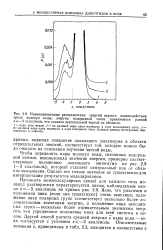 |
Нормализованные распределения энергий парного взаимодействия среди молекул воды. энергия водородной связи принимается равной е - 3 ккал / моль, что указано вертикальной чертой на абсциссе. [30] |
Страницы: 1 2 3 4 5