Сложноэфирная связь
Cтраница 3
При использовании реагентов со сложноэфирной связью исследовано множество радикальных реакций: хлорирование хлориодфенил-радикалами, нитрозирование по реакции Бар-тона и отщепление водорода действием триплетного бензофенона, приводящее к ненасыщенности или замыканию цикла с образованием гидроксилактона. В случае ( 139) возможности фотоциклизации практически ограничены атомами С-11 ( 65 %) и С-10 ( 28 %) остатка спирта. Очевидно, что такие интересные реакции наиболее перспективны для стероидных спиртов. [31]
Поскольку эти соединения благодаря наличию сложноэфирной связи Р - О-С в ряде случаев оказываются способными к реакциям гидролиза. [32]
Известно, что скорость гидролиза сложноэфирной связи в водном растворе щелочного агента с повышением температуры значительно возрастает. Однако установлено [176], что она зависит от концентрации щелочного агента и, если последняя не превышает 3 - 4 % ( масс.), то даже при температуре выше 100 С степень гидролиза эфира при нейтрализации невелика. Вначале эфир-сырец смешивают с водным раствором щелочного агента при 60 - 80 С. При смешении нейтрализация завершается на 70 - 80 % и концентрация свободной щелочи в реакционной массе резко падает. Далее образующуюся дисперсную систему нагревают до температуры кипения водного раствора щелочи и нейтрализация завершается при непрерывной гетероазеотропной отгонке водно-спиртовой паровой смеси. Пары воды и спирта, образующиеся при кипении, конденсируются и охлаждаются в холодильнике. Конденсат расслаивается во флорентийском сосуде на спирт и воду. Вода непрерывно возвращается в нейтрализатор, а спирт отделяется для последующего использования на стадии этерификации. [33]
В тейхоевых кислотах доказано наличие сложноэфирной связи ( тип А) аланина с остатками рибита. Высказано предположение о наличии в гликопротеинах О-ацилгликозид-ной связи, однако твердые доказательства существования такого типа связи еще отсутствуют. Очевидно, в сложных по структуре гликопротеинах углеводные и пептидные части могут быть связаны и несколькими разными типами связей, о чем свидетельствует неполное расщепление всех гликопептидных связей под действием какого-либо одного реагента и образование смеси низкомолекулярных гл и ко пептидов, содержащих связи разного типа при неспецифической деструкции исходного гликопротеина. [34]
При деструкции полиэфиров происходит разрыв сложноэфирных связей макромолекул. Принцип, согласно которому большинство исследователей подбирают стабилизаторы для ПЭТФ, основан, как правило, на блокировании наиболее неустойчивых концевых гидроксильных групп полиэфира. Исходя из вышесказанного, можно было ожидать, что красители арлламиноантрахинонового ряда с активными концевыми группами, вступая в реакцию с полимером, должны оказывать термостабилизирующее действие на цветные полиэфиры и волокна. Краситель с одной функциональной группой, вставая на конец цепи, будет блокировать концевую гидроксильную группу; а краситель с двумя функциональными группами, вступая в середину цепи, должен упрочнять ее за счет образования простой эфирной связи. [35]
Алифатическая гидроксильная группа, расположенная возле сложноэфирной связи, может способствовать щелочному гидролизу последней. [36]
В обычных липидах глицерол связан сложноэфирной связью с жирными кислотами, а у архей - простой эфирной связью с С2о - сциртом - фитано-лом. Такие эфиры могут образовывать тетрамеры ( С40), а цепи фитанола могут содержать пятичленные кольца. Археи могут иметь как обычные бислойные, так и ригидные монослойные мембраны, но чем экстремальнее условия, тем больше монослойных областей находится в мембране. [37]
Считают, что между ними возникает сложноэфирная связь в а-по-ложении. Эта связь образуется за счет гидроксилов бензилового спирта лигнина и карбоксильных групп уроновых кислот. [38]
Сложные полиэфиры характеризуются наличием в молекуле сложноэфирной связи. [39]
Полученные нами предварительные данные по устойчивости сложноэфирной связи аминоациальных производных глюкозы показывают, что они могут оказаться полезными при доказательстве наличия сложноэфирной связи между белковой и углеводной компонентами мукополисахаридов. [40]
Основной химический процесс - частичный гидролиз сложноэфирных связей в ксантогенате целлюлозы, приводящий к понижению степени замещения. [41]
С-концевого остатка серина этого пептида образует сложноэфирную связь с карбоксильной группой остатков лизина или аргинина в гликопротеине. Тетрадекапептид может также быть расщеплен in vitro с образованием ангиотензина I. Ни тетрадекапептид, ни декапептид не проявляют гипертензивных свойств. [42]
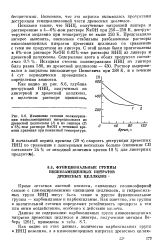 |
Изменение степени полимеризации низКозамещенных нитроцеллюлоз из древесной целлюлозы ( 7 и из линтера ( 2 в 6 % - ном растворе NaOH с течением времени хранения при комнатной температуре. [43] |
Кроме остатков азотной кислоты, связанных сложноэфирной связью с глюкопиранозньтми единицами целлюлозы, и гидроксиль-ных групп ННЦ могут быть также и другие функциональные группы - карбонильные и карбоксильные. Как известно, эти группы в значительной степени определяют устойчивость препарата к тем или иным воздействиям, особенно к действию щелочи. [44]
Во всех рассмотренных до сих пор примерах сложноэфирная связь была расположена в пара - положении по отношению к оставшейся свободной карбоксильной группе, поэтому такие вещества называют / ш / ш-депсидами. В лишайниках и грибах они подвергаются довольно сложному метаболизму, порождая лшшг-депсиды, дифениловые эфиры, депсидоны и дибензофураны. [45]
Страницы: 1 2 3 4