Четвертая связь
Cтраница 1
Четвертая связь, перпендикулярная плоскости страницы, показана точкой внутри буквы С. [1]
Четвертая связь каждого атома направлена перпендикулярно плоскости трех других связей и соединяет между собой атомы разных плоскостей. Расположение атомов в каждой из плоскостей можно представить как сплошное заполнение плоскости правильными шестиугольниками, в вершинах которых лежат углеродные атомы. Четвертая связь имеет большую длину, чем три остальных, и значительно слабее их. [2]
Четвертая связь центрального углеродного атома ( не занятая фенильными группами) значительно отличается от нормальных связей углерода. Атомы и радикалы, связанные этой связью, очень подвижны. Эта связь больше походит на электровалентную, чем а ковалентную: производные трифенилметана с заместителями при центральном атоме углерода обнаруживают тенденцию к ионизации. [3]
Направление четвертой связи не устанавливается. Очевидно, что в формуле Ладенбурга расположение связей, исходящих из атома углерода, таково, что они направлены к вершинам неправильного тетраэдра, хотя это и не подчеркивается самим автором формулы. Как бы там ни было, формулу Ладенбурга для бензола следует рассматривать как первую структурную формулу в пространстве. [4]
Хотя эта четвертая связь N - Н образовалась иначе, чем три первые связи, но по природе она становится не отличимой от первых трех. [5]
Когда бор образует четвертую связь, все связи упрочняются ( все связывающие орбиты становятся тетраэдрическими), и молекула делается более устойчивой. [6]
Ионизация окупается за счет образования четвертой связи, гибридизации и упрочения всех гибридных связей. [7]
Из этой формулы видно, что четвертая связь разделена поровну между атомами кислорода. [8]
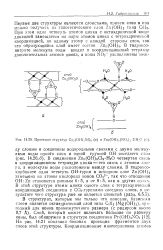 |
Проекции структур Cu2 ( OH 3NO3 ( а и Zn5 ( OH3 ( NO3h - 2 H. O ( о. [9] |
В соединении Zn5 ( OH) 8Cl2 - H20 четвертая связь в координационном тетраэдре цинка - это связь с атомом хлора, а молекулы воды расположены между слоями. В гидроксо-карбонате одна четверть ОН-групп в исходном слое Zn ( OH) 2 замещена на атомы кислорода ионов СО32 -, так что отношение ОН: Zn становится равным 6: 5, а не 8: 5, как в других солях. В этой структуре атомы цинка одного слоя с тетраэдрической координацией соединены с С03 - группами соседних слоев, в результате чего структура уже не является слоистой ( разд. На рис. 14.21 показана боковая проекция фрагментов двух слоев этой структуры. [10]
С - Н должны быть взаимно перпендикулярными, а четвертая связь не должна иметь определенного направления в пространстве. Другими словами, одинаково сильное ( или слабое) перекрывание может быть обеспечено независимо от того, где расположен четвертый атом водорода относительно трех остальных. С другой стороны, можно ожидать, что отталкивание между атомами водорода должно вызывать удаление этого четвертого атома на возможно большее расстояние, так что четвертая связь должна быть слабее трех остальных и отличаться от них по длине. [11]
В структурной формуле бензола, приведенной выше, отсутствует четвертая связь углеродных атомов. [12]
Активный комплекс можно представить себе как молекулу, в которой четвертая связь углерода резонирует между ионами гидроксила и иода. [13]
В противном случае связывание металла с пептидным азотом подразумевает образование четвертой связи с изменением тригональной гибридизации sp2 в тетраэдрическую sp3 и потерю резонанса пептидной группы. Еще до того, как было установлено это правило, были предложены структурные формулы, показывающие связывание металла атомами азота протонированных пептидных групп. Однако в свете изложенного все эти формулы должны быть пересмотрены. [14]
Неподеленная пара электронов в молекулах типа МНз может использоваться для образования четвертой связи - координационной ( -) по Сиджвику, например, в аминах металлов ( см. координационные соединения Вернера, гл. [15]
Страницы: 1 2 3 4