Фосфоэфирная связь
Cтраница 2
В случае неприродной межнуклеозидной фосфодиэфирной связи рядом с символом межнуклеотидной связи в скобках указываются номера атомов, при которых находятся гидроксильные группы, образующие фосфоэфирную связь. [16]
В том случае, если а-диольная группа принадлежит нуклеозид-5 - фосфату, олиго - или полинуклеотиду, окисление с последующей обработкой щелочью или аминами приводит к расщеплению фосфоэфирной связи с одновременным отщеплением основания. Реакция дает возможность избирательно отщеплять 3 -концевые звенья у полирибонуклеотидов и используется при анализе последовательности РНК. [17]
В поисках оптимальных условий проведения реакции изучалось влияние ряда аминокислот и первичных аминов ( глицина, аспара-гина, лизина, метиламина, циклогексиламина) 177 - 182, рН среды 8 - 181 температуры ш на скорость расщепления фосфоэфирной связи в диальдегидах, полученных периодатным окислением рибо-нуклеозид-5 - фосфатов и ряда олигонуклеотидов со свободной концевой 1 с-гликольной группировкой. Данные о влиянии рН на скорость распада фосфоэфирной связи противоречивы. [18]
Значительно большую лабильность фосфоэфирных связей в амиде Буклеозид-3 5 -циклофосфата по сравнению с соответствующим незамещенным циклофосфатом можно объяснить двумя причинами: во-первых, в полностью замещенном фосфате облегчена атака фосфора молекулой воды или другим нуклеофильным реагентом; во-вторых, при замене кислорода в диэфире фосфорной кислоты на азот, неподеленная пара электронов которого, как известно, способна участвовать в сопряжении в большей степени, чем неподеленная электронная пара кислорода, уменьшается сопряжение Sd-орбит фосфора с эфирным кислородом, в результате чего фосфоэфирная связь ( Р - OR) ослабляется. [19]
Из панкреатической железы была выделена рибонуклеаза, полученная в 1940 г. в кристаллическом состоянии. Она действует на РНК, расщепляя фосфоэфирную связь присоединенного к положению 3 пиримидинового нуклеозида ( см. гл. [20]
В поисках оптимальных условий проведения реакции изучалось влияние ряда аминокислот и первичных аминов ( глицина, аспара-гина, лизина, метиламина, циклогексиламина) 177 - 182, рН среды 8 - 181 температуры ш на скорость расщепления фосфоэфирной связи в диальдегидах, полученных периодатным окислением рибо-нуклеозид-5 - фосфатов и ряда олигонуклеотидов со свободной концевой 1 с-гликольной группировкой. Данные о влиянии рН на скорость распада фосфоэфирной связи противоречивы. [21]
Если принять во внимание способ образования нуклеиновых кислот при биосинтезе ( т.е. синтезе в живых организмах или с помощью ферментных систем, выделенных из живых организмов), то их следует рассматривать как полимеры, образованные нуклеозид-5 - фосфатами. При этом каждый остаток фосфорной кислоты мономера, кроме концевого, связан фосфоэфирной связью с 3 - ОН-груп-пой соседнего мономерного звена. На рис. 7 приведена структура примыкающих к концам фрагментов нуклеиновой кислоты с некоторой произвольной последовательностью нуклеотидов. Видно, что все остатки фосфорной кислоты, кроме одного, образуют фосфодиэфирные группы и все 3 -гидроксигруппы, кроме одной, участвуют в образовании фосфоэфирных связей. Остаток, содержащий 5 -фосфомоноэфирную группу, называют 5 -концевым, а остаток, содержащий не-этерифицированную 3 -гидроксигруппу, - 3 -концевым. [22]
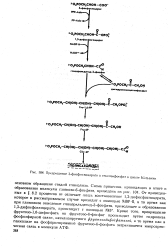 |
Превращение 3-фосфоглицерата в гексозофосфат в цикле Кальвина. [23] |
От приведенных в § 8.2 процессов ее отличает лишь восстановление 1 3-дпфосфоглицерата, которое в рассматриваемом случае проходит. Кроме того, превращение фруктозо-1 6-дифосфата во фруктозо-6 - фосфат ггроисходит путем гидролиза фосфоэфирной связи, катализируемого фруктозодифосфатазой, в то время как в гликолизе на фосфорилнрование фруктозо - С-фосфата затрачивается макроэрги-ческая связь в молекуле АТФ. [24]
При осуществлении синтеза этих соединений следует считаться с возможностью миграции фосфатного остатка [189], а также с ацильной миграцией [190] при использовании сложноэфирных защитных групп в миоинозитном кольце. К защитным группам предъявляется ряд требований: возможность селективного введения, удаление без разрыва фосфоэфирных связей и с сохранением функциональных групп в глицериновой половине молекулы. [25]
В отношении дальнейшей судьбы мононуклеотидов в кишечнике существует два предположения. Во-первых, мононуклеотиды расщепляются под действием неспецифических фосфатаз ( кислой и щелочной), которые гидролизу-ют фосфоэфирную связь ( нуклеотидазное действие) с образованием нукле-озидов и фосфорной кислоты, и в таком виде всасываются. Второе предположение заключается в том, что мононуклеотиды всасываются и распад их осуществляется в клетках слизистой оболочки кишечника. Имеются также доказательства существования в стенке кишечника нуклеотидаз, катализирующих гидролитический распад мононуклеотидов. Дальнейший распад образовавшихся нуклеозидов осуществляется внутри клеток слизистой преимущественно фосфорилитическим, а не гидролитическим путем. [26]
В отношении дальнейшей судьбы мононуклеотидов существует два предположения. Считают, что мононуклеотиды в кишечнике под действием неспецифических фосфатаз ( кислой и щелочной), которые гидролизируют фосфоэфирную связь мононуклеотида ( нуклеотидазное действие), расщепляются с образованием нуклеозидов и фосфорной кислоты и в таком виде всасываются. Согласно второму предположению, мононуклеотиды всасываются, а распад их происходит в клетках слизистой оболочки кишечника. Имеются также доказательства существования в стенке кишечника нуклеотидаз, катализирующих гидролитический распад мононуклеотидов. [27]
Он имеет молекулярную массу около 10 Ша; сравнительно термостабилен; содержит фосфорилированную пан-тотеновую кислоту ( витамин В3) и тиоэтиламин, ковалентно присоединенные к полипептидной цепи АПБ через сериновый остаток фосфоэфирной связью. [28]
Итак, организация белковой молекулы происходит в результате различного рода молекулярных взаимодействий, которые и определяют уровни ее структуры. Первичная структура макромолекулы белка целиком определяется ковалентными связями вдоль полипептидной цепи, вторичная - водородными связями между пептидными группами, расположенными в соседних витках спирали или соседних участках разных цепей, и, наконец, третичная структура - химическими сшивками отдельных участков одной цепи или нескольких цепей ( дисульфидные мостики, фосфоэфирная связь) и силами взаимодействия неполярных боковых радикалов некоторых аминокислот. [29]
Реакции, приводящие к расщеплению фосфоэфирных ( в особенности фосфодиэфирных) связей, занимают особое место в ряду других химических превращений нуклеиновых кислот и их компонентов. Они являются основой аналитических методов, используемых для определения состава и строения нуклеиновых кислот. Хотя в настоящее время химические методы гидролиза фосфоэфирных связей в значительной степени уступили место ферментативным, позволяющим проводить такое расщепление в более мягких условиях и более специфично, тем не менее возможности химических способов гидролиза еще далеко не исчерпаны. [30]
Страницы: 1 2 3