Аллильная двойная связь
Cтраница 1
Аллильная двойная связь 2-алкениланилина в щелочных условиях претерпевает сдвиг к ароматическому кольцу, образовывая производные замещенного стирола. Это свойство - несомненное преимущество аминоарилзамещенных алкенов, поскольку увеличиваются синтетические возможности этих аминов. Наиболее простым, удобным и препаративным лабораторным способом, на наш взгляд, является термическая изомеризация аминоарилал-кенов. [1]
Аллильная двойная связь 2-алкениланшшна в щелочных условиях претерпевает сдвиг к ароматическому кольцу, образовывая производные замещенного стирола. Это свойство - несомненное преимущество аминоарилзамещенных алкенов, поскольку увеличиваются синтетические возможности этих аминов. Наиболее простым, удобным и препаративным лабораторным способом, на наш взгляд, является термическая изомеризация аминоарилал-кенов. [2]
Побочные р-ции-миграция аллильной двойной связи в а, р-положение к карбонилу ( напр. [3]
Так как все эти группы могут взаимодействовать с аллильной двойной связью посредством резонанса или гиперконъюгации, и, следовательно, переходное состояние должно быть стабилизованным, нельзя сделать никаких определенных выводов относительно влияния индуктивных эффектов этих групп на реакционную способность. К тому же как y - mpem - бутильная группа, так и у-трифторметильная группа ( из которых ни одна не может взаимодействовать мезомерно с реакционным центром) увеличивают SN2 реакционную способность. [4]
Для связывания 13 3-аллил - и 11 3-оксигруппы необходимо было предварительно окислить аллильную двойную связь. [5]
Аллиловые эфиры энергично реагируют с галогенами, в частности - с хлором или бромом с присоединением последних по месту аллильной двойной связи и образованием дигалоидгидринов моноглицеридов. Затем атомы галоидов в дигалоидгидрине могут быть замещены на кислотные остатки при действии соли органической кислоты с образованием однокислотных или смешанно-кислотных триглицеридов. [6]
Большая термодинамическая устойчивость у-алкильного члена первично-вторичной или первично-третичной пары изомерных аллильных галогенпроизводных, вероятно, обусловливается гиперконъюгационным взаимодействием алкильной группы с аллильной двойной связью. [7]
Большая термодинамическая устойчивость Y-ЭЛКИЛЬНОГО члена лервично-вторич-ной или первично-третичной пары изомерных аллильных галогенпроизводных, вероятно, обусловливается гиперконъюгационным взаимодействием алкильной группы с аллильной двойной связью. [8]
Насколько известно, такие илиды в реакции Виттига реагируют исключительно поа-углеродному атому, однако резонансный эффект, очевидно, имеет место в некоторых случаях при цис-транс-язоме-ризации аллильной двойной связи, которая происходит более или менее легко при комнатной температуре. [9]
Морфин и а-изоморфин, а также кодеин и изокодеин ( см. схему 34) являются Сб-эпимерными спиртами. Подобное соотношение при Се с аллильной двойной связью Д6 7 имеет место для р - и у-изоморфинов и соответственно аллопсевдокодеина и псевдокодеина. [10]
Показано, что чувствительность двойных связей по отношению к грег - ВиОгН может изменяться в зависимости от используемого катализатора. Так, если катализатором является ванадий, аллильная двойная связь эпоксидируется легче винильной. [11]
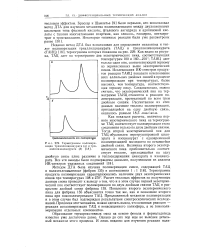 |
Термограммы полимери. [12] |
ТАИЦ дает только один пик, соответствующий первому из перечисленных выше экзотермических пиков. Исследования ИК-спектров продуктов реакции ТАИЦ показали исчезновение всех аллильных двойных связей в процессе полимеризации при температурах, более высоких, чем температура, соответствующая первому пику. Следовательно, можно считать, что экзотермический пик на термограмме ТАИЦ относится к реакции полимеризации, протекающей по всем трем двойным связям. Рассчитанное из этих данных значение теплоты полимеризации, приходящейся на одну двойную связь, оказалось равным 18 5 ккал / моль. [13]
По отношению к алкилирующим и ацилирующим агентам, а также в реакции образования оснований Шиффа с альдегидами аллиламин ( 55) проявляет себя как типичный амин. Азометино-вая двойная связь в основаниях Шиффа может быть восстановлена с помощью алюминиевой фольги, активированной хлоридом ртути ( II) ( уравнение 27) [64], или водородом в присутствии никеля Ренея ( уравнение 28) [65]; аллильная двойная связь при этом сохраняется. [14]
Из данных табл. 2 следует, что и электроноакцепторные, и электронодонорные у-заместители облегчают реакции аллильных хлоридов с йодистым калием в ацетоне и с этилатом натрия в этаноле. Заместители - галоген, алкил, арил, циан и сульфонил - ускоряют аллильные SN2 реакции, и влияние двух заместителей неизменно больше, чем влияние одного из них. Так как все эти группы могут взаимодействовать с аллильной двойной связью посредством резонанса или гиперконъюгации, и, следовательно, переходное состояние должно быть стабилизованным, нельзя сделать никаких определенных выводов относительно влияния индуктивных эффектов этих групп на реакционную способность. К тому же как y - mpem - бутильная группа, так и у-трифторметильная группа ( из которых ни одна не может взаимодействовать мезомерно с реакционным центром) увеличивают 5 2 реакционную способность. [15]
Страницы: 1 2