Тройная связь
Cтраница 2
Тройная связь старше двойной. [16]
Тройная связь может быть введена в любой цикл, начиная с пятичленного. Индивидуально существуют только соединения, начиная с циклооктина. Однако, как показал Виттиг, углеводороды с тройной связью в 5 -, 6 - и 7-членном циклах могут вступать в различные реакции в момент образования, обычно при низких температурах. [17]
Тройная связь может быть введена в любой цикл, начиная с пя-тичленного. Индивидуально существуют только соединения, начиная с циклооктина. Однако, как показал Виттиг, углеводороды с тройной связью в 5 -, 6 - и 7-членном циклах могут вступать в различные реакции в момент образования, обычно при низких температурах. [18]
Тройная связь, однако, изображению с помощью такой модели не поддавалась, и Льюису пришлось ввести дополнительно к кубической модели атома еще и тетраэдрическую. [19]
Тройная связь менее реакционноспособна, чем двойная. Это различие, вероятно, можно приписать более жесткой структуре промежуточного радикала, неизбежно содержащего двойную связь, или же более напряженной конфигурации промежуточного комплекса. [20]
 |
Схема иллюстрирует связь между высокой реакционной способностью аллилхлорида в реакциях SN. по сравнению с - пропилхлоридом и низкой энергией образования аллил-катиона. [21] |
Тройная связь оказывает сравнимое по силе влияние; показано, например, что хлор в З - хлорпропине-1 очень подвижен. [22]
Тройная связь азот - углерод существенно отличается от углерод-углеродной тройной связи - она обладает большей прочностью ( 212 и 200 ккал соответственно) и гораздо большей полярностью. На высокую степень полярности тройной связи углерод - азот указывает большое значение дипольного момента ( 4 0 Д) простых нитрилов ( RCN); эта величина составляет приблизительно 70 % от величины дипольного момента, которой следовало бы ожидать в том случае, если одна из связей, входящих в состав тройной связи, была бы полностью ионной. Не удивительно поэтому, что жидкие нитрилы имеют довольно высокие диэлектрические проницаемости по сравнению с большинством жидких органических соединений и весьма хорошо растворимы в воде. [23]
Тройная связь азот - азот является наиболее прочной из всех известных ко-валентных связей. Ряд молекул, электронное строение которых может рассматриваться таким же, как у азота ( иначе говоря, соединения, нзоэлектронные с азотом), обладают устойчивостью, несмотря на то что они, казалось бы, нарушают простые правила валентности. Наиболее ярким примером такого соединения может служить окись углерода; ее устойчивость можно объяснить, исходя из наличия двух резонансных структур, в одной из которых имеется тройная связь, аналогичная связи в молекуле азота. [24]
 |
Схема иллюстрирует связь между высокой реакционной способностью аллил-хлорида в реакциях SN. по сравнению с к-пропилхлоридом и низкой энергией образования аллил-катиона. [25] |
Тройная связь оказывает сравнимое по силе влияние; показано, например, что хлор в З - хлорпрошше-1 очень подвижен. [26]
Тройная связь образуется одной з-связью с электронным облаком по линии связи и двумя - - связями в двух взаимно перпендикулярных плоскостях. [27]
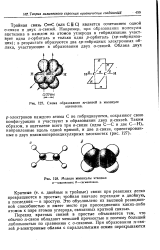 |
Схема образования я-связей в молекуле ацетилена.| Модели молекулы этилена. а - шариковая. б сегментовая. [28] |
Тройная связь С С ( или С 5 С) является сочетанием одной о-связи и двух я-связей. Например, при образовании молекулы ацетилена в каждом из атомов углерода в гибридизации участвует одна s - орбиталь и только одна р-орбиталь ( sp - гибридиза-ция); в результате образуются два sp - гибридных электронных облака, участвующие в образовании двух а-связей. [29]
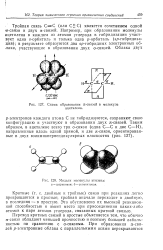 |
Схема образования it - связей в молекуле ацетилена.| Модели молекулы этилена. а - шариковая. б - сегмептовая. [30] |
Страницы: 1 2 3 4 5