Тройная связь
Cтраница 4
Тройная связь ( в стеароловой кислоте), удаленная от головной группы, дает настолько сильное притяжение к воде при небольшом увеличении боковой когезии между цепями, что пленки являются парообразно-растянутыми. Эта тройная связь вызывает значительное повышение скачка потенциала. [46]
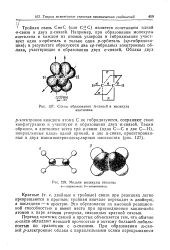 |
Схема образования я-связей в молекуле ацетилена.| Модели молекулы этилена. [47] |
Тройная связь С С ( или С С) является сочетанием одной о-связи и двух л-связей. [48]
Тройная связь дает экзальтацию - 2 336 Таким образом, величина экзальтации позволяет определить число этиленовых или иных связей в рассматриваемом соединении. [49]
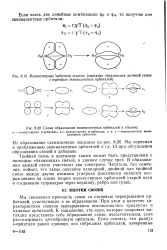 |
Молекулярные орбита ли этилена ( описание образования двойной связи с помощью эквивалентных орбиталей.| Схема образования эквивалентных орбиталей в этилене. [50] |
Тройная связь в ацетилене также может быть представлена с помощью банановых связей, в данном случае трех. В образовании каждой связи участвуют два электрона. Читатель, без сомнения, поймет, что такое описание одинарной, двойной или тройной связи между двумя атомами углерода фактически является возрождением а языке теории молекулярных орбиталей старой идеи о соединении тетраэдров через вершину, ребро или грань. [51]
Тройная связь - связь между двумя атомами, осуществляемая тремя парами электронов. [52]
Тройная связь укорачивает расстояние в группе СС, меняя эффективность л-сопряжения. Тройная связь повышает также жесткость скелета, что способствует появлению фосфоресценции; молекулы с сопряженными двойными связями ( стирол, дифенилполиены) обычно не фосфоресцируют. [53]
 |
Схемы образования я-связи и электронного строения двойной связи.| Схемы образования двух л-связей и электронного строения тройной. [54] |
Тройная связь С С осуществляется тремя парами обобщенных электронов С:: С ( с. Состояние этих пар не одинаково, так же как и в случае двойной связи: одна из них представляет собой а-связь, две другие - л-связи. У каждого углеродного атома образуются два гибридных состояния, а два р-состояния не участвуют в гибридизации и сохраняют свою конфигурацию. [55]
Тройная связь, так же как и двойная, по характеру отличается от простой связи. Этим обусловливаются реакции присоединения по месту тройной связи. Последние идут ступенчато: вначале тройная связь разрывается, превращаясь в двойную, и образуются производные этиленовых углеводородов; затем разрывается и двойная связь, превращаясь в простую с образованием производных предельных углеводородов. При энергичном химическом воздействии возможен распад молекул с разрывом углеродной цепи по месту тройной связи. [56]
Тройная связь окисляется труднее, чем двойная; это позволяет избирательно окислять двойную связь в присутствии тройной. Окислительные реагенты могут быть использованы те же, но в более жестких условиях. [57]
Тройная связь окисляется труднее, чем двойная; это позволяет избирательно окислять двойную связь в присутствии тройной, так как тройная связь окисляется в более жестких условиях. [58]
Тройная связь в молекуле N2 очень прочна. [59]
Тройная связь в N2 обладает повышенной устойчивостью также к реакциям присоединения; это связано с неполярностью молекулы N2 и ее высоким потенциалом ионизации. Напротив, группы - С С - и - C N проявляют я-электронодонорные свойства. В последние годы было показано, что и молекула N2 может выступать в качестве я-донорноголиганда, образуя комплексы при нормальных условиях. [60]
Страницы: 1 2 3 4 5