Банановая связь
Cтраница 1
Банановая связь ( Т - связь) - связь а-типа, не имеющая максимального перекрывания атомных орбиталей, составляющих эту связь, поскольку они не направлены вдоль межъядерной оси. Такая связь существует, в частности, между атомами углерода в циклопропане. [1]
Однако в действительности в этих реакциях также имеет место разрушение банановых связей, превращение их в нормальные электро-нонедефицитные связи. Соединения типа Me1 [ BHJ называются боранатами или гидроборатами. Гидробораты известны для щелочных, щелочно-земельных и некоторых других металлов. В практике чаще других используется NafBHJ - белое нелетучее вещество, устойчивое в сухом воздухе. Он растворяется в воде и органических растворителях. [2]
Однако в действительности в этих реакциях также имеет место разрушение банановых связей, превращение их в нормальные электрононедефицитные связи. [3]
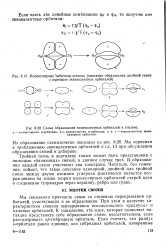 |
Молекулярные орбита ли этилена ( описание образования двойной связи с помощью эквивалентных орбиталей.| Схема образования эквивалентных орбиталей в этилене. [4] |
Тройная связь в ацетилене также может быть представлена с помощью банановых связей, в данном случае трех. В образовании каждой связи участвуют два электрона. Читатель, без сомнения, поймет, что такое описание одинарной, двойной или тройной связи между двумя атомами углерода фактически является возрождением а языке теории молекулярных орбиталей старой идеи о соединении тетраэдров через вершину, ребро или грань. [5]
Своеобразные свойства циклопропанового кольца, как уже упоминалось, связывают с особым состоянием гибридизации составляющих его углеродных атомов, с наличием банановых связей в циклопропане. Эти же причины оказывают определенное влияние и на стереохимию реакций замещения в циклопропане. [6]
 |
Строение молекулы дибо-рана В2Н6.| Мостиковые орбитали в В2Н6. [7] |
В ней два электрона ( один от водорода, а другой от одного атома бора) обслуживают три центра - два атома бора и один атом водорода. Именно в банановой связи наблюдается дефицит электронов: на четыре связи приходится столько же электронов. [8]
В ней два электрона ( один - от водорода, а другой - от одного атома бора) обслуживают три центра: два атома бора и один атом водорода. Именно в банановых связях наблюдается дефицит электронов: на четыре связи приходится столько же электронов. [9]
Наиболее реакционноспособными являются спиродиеноны типа XXII, содержащие циклопропановое кольцо. Повышенная реакционная способность подобных соединений является следствием сопряжения банановых связей циклопропана с системой циклогек-садиенона. Подобному сопряжению максимально способствует пространственное расположение обеих частей молекулы, так как трехчленный цикл в этих соединениях жестко закреплен перпендикулярно плоскости циклогексадиенона. [10]
Лонге-Хиггинс показал, что можно перегруппировать использованные Питцером орбитальные функции таким образом, чтобы получить альтернативное описание диборана. В этом описании две группы ВН2 соединяются двумя эквивалентными трех-центровыми или банановыми связями, каждая из которых охватывает два атома бора и один из мостиковых атомов водорода. Эти эквивалентные орбитали напоминают рассмотренные ранее орбитали этилена ( см. с. [11]
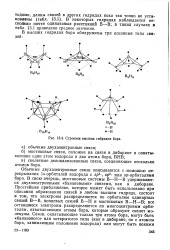 |
Строение высших гибридов бора. [12] |
Обычные двухэлектронные связи описываются с - помощью перекрывания ls - орбиталей водорода с sp3 -, sp2 - или sp - орбиталями бора. В свою очередь, мостиковые системы В - Н - В удерживаются двухэлектронными банановыми связями, как в диборане. Простейшее приближение, которое может быть использовано при описании образования связей в любом высшем гидриде, состоит в том, что электроны распределяются по орбиталям одинарных связей В-В, концевых связей В - Н и мостиковых В - Н - В; все оставшиеся электроны распределяются по многоцентровым орбиталям, охватывающим атомы бора, которые образуют скелет молекулы. [13]
Точно такой же подход может быть применен для этилена или ацетилена. Как указал Леннард-Джонс, возможно альтернативное представление в виде эквивалентных орбит, когда связь С С образуется из двух изогнутых а-связей ( банановая связь) с помощью нелинейного пере крывания ( рис. 3, б); эти представления совершенно равнозначны и в каждом из них шесть эквивалентных орбит взаимодействуют друг с другом довольно слабо. [14]
Напряженность молекулы циклопропана объясняется главным образом ненормальными углами между С - С-связями - взаимным отталкиванием электронных облаков этих связей. Несмотря на то что при подобном искажении электронного облака перекрывание становится менее полным, такое расположение связей оказывается энергетически более выгодным. Циклопропан Они носят название банановых связей ( бананооб - и его банановые разное электронное облако искаженной о-связи) и, связи. [15]
Страницы: 1 2