Слабая химическая связь
Cтраница 2
Следует заметить, что величина и0 существенно ниже, чем прочность любой наиболее слабой химической связи в исследованных полимерах. [17]
 |
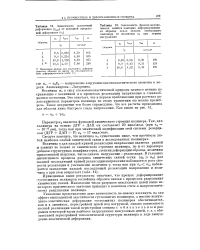
Сандвичеобразная структура ферроцена. [18] |
Мы, конечно, не утверждаем, что все сандвичеобразные соединения обладают слабыми химическими связями, однако считаем, что удобнее всего обсуждать структуру таких соединений именно в этом месте книги. [19]
Конрадсону и энергией активации, показано, что вязкое течение связано с образованием и разрывом слабых химических связей. [20]
Механизм термического сольволиза MOB определяется температурным интервалом их термодеструкции и реакционной способностью образующихся при разрыве наиболее слабых химических связей свободных радикалов. Радикальные продукты термолиза углей по реакции, конкурирующей с реакцией образования кокса, стабилизируются подвижным водородом растворителя. В то же время высокоактивные алкильные радикалы, получающиеся при термодеструкции каучуков при более низких температурах, легко вступают во внутримолекулярные реакции передачи цепи и циклизации и не реагируют с донорами водорода. Железосодержащие катализаторы не оказывают активирующего влияния на термический распад химических связей в макромолекулах газового угля и резины, но ускоряют термический сольволиз бурых углей с более слабыми С - О связями. Более заметно влияние этого типа катализаторов на вторичные реакции продуктов терморастворения углей, асфальтенов и масел. [21]
По нашему мнению, пар водного раствора аммиака должен рассматриваться как двухкомпонентная газовая смесь с весьма слабой химической связью между молекулами воды и аммиака. [22]
Последние данные относятся к квазихрупкому разрушению с энергией активации, соответствующей разрыву одной полимерной цепи по слабой химической связи С - С. Раньше считалось, что эти данные относятся к хрупкому разрушению. Следует указать, что большинство данных по долговечности относится к квазихрупкому, а выше Гкхр - к нехрупкому, или пластическому разрушению с образованием и ростом квазихрупких микротрещин и крейзов. Регель [5.21] делает вывод в отношении пластмасс, что Временная зависимость прочности в основном связана с закономерностями роста трещин, а не возникновением новых зародышей трещин. К такому же выводу пришли Журков и То-машевский [2.6] при исследовании процесса роста хрупкой трещины в пластмассах. В отношении волокон дело обстоит сложнее, так как существенным этапом разрушения является зарождение под нагрузкой субмикротрещин. [23]
На расстояниях, меньших, чем сумма ван-дер-ваальсовых радиусов взаимодействующих молекул, между последними возможно образование слабых химических связей. Различие между сильными и слабыми химическими связями в основном количественные, а именно: энергия образования слабых связей на 1 - 2 порядка ниже энергии образования ковалентной связи. Одной из основных форм слабых взаимодействий являются водородные связи, обозначаемые X - H... [24]
Нагревание каучуков ( и вулканизатов) выше некоторого температурного предела приводит к распаду ( пиролизу) наиболее слабых химических связей с образованием свободных радикалов, вызывающих цепной процесс полимеризации и деструкции. [25]
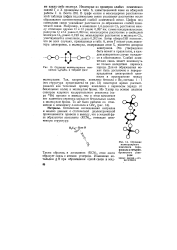 |
Строение молекулярного комплекса С8НеВг2 в твердой фазе. [26] |
В графе связи и межъядерные расстояния этой таблицы цифры над символами связи указывают расстояния после образования соответствующей слабой химической связи. Цифры под символами связи указывают расстояния до образования слабой химической связи. Например, в комплексе 1 4-диоксан С12 расстояние между атомными ядрами О и С1 равно 0 267 нм; сумма вандерваальсовых радиусов О и С1 равна 0 320 нм; межъядерное расстояние в свободной молекуле С12 равно 0 199 нм; межъядерное расстояние в молекуле С12, участвующей в комплексе, равно 0 202 им. [27]
Итак, наши расчеты показывают, что возникновение активного комплекса в растворах может сопровождаться разрывом небольшого числа слабых химических связей между молекулами растворителя. Энергия активации, по крайней мере в тех случаях, когда наблюдается изокинетический эффект, возникает за счет химической энергии межмолекулярных взаимодействий в растворах. Рост энергии активации сопровождается увеличением числа разрушающихся слабых связей между молекулами растворителя, возрастанием числа поступательных степеней свободы. Потенциальная энергия слабых химических связей превращается в кинетическую энергию поступательного движения молекул, избыток которой переходит в энергию возбуждения активного комплекса. [28]
В биологических системах переход из жидкого состояния в твердое всегда бывает связан с критической стабилизацией большого числа слабых химических связей. С уменьшением кинетической энергии молекул воды взаимодействия между ними, обусловленные водородными связями, становятся более стабильными, и при снижении температуры ниже определенного уровня образуется лед. Менее изучены переходы из жидкого состояния в твердое в случае липидов. Понижение температуры и здесь приводит к повышению стабильности слабых связей, и в конце концов происходит затвердевание. [29]
Что касается отношения Ti / P / т ег увеличение наблюдается при переходе к соединениям, характеризующимся слабыми химическими связями и содержащими большие по размерам, легкополяризуемые ионы. [30]
Страницы: 1 2 3 4