Ионная химическая связь
Cтраница 1
Ионная химическая связь - предельный случай полярности химической ковалентной связи, которому отвечает значительное смещение пары электронов связи к наиболее электроотрицательному атому. Этот атом приобретает отрицательный заряд и превращается в анион. Другой атом, лишившись своего электрона, образует катион. Иногда механизм ионной химической связи называют гарпунным механизмом. Более электроположительный атом как бы забрасывает свой электрон на более электроотрицательный атом и подтягивает его к себе за счет электрического взаимодействия образовавшихся ионов. [1]
Ионная химическая связь не обладает насыщаемостью, не имеет направленности и повышенной электронной плотности в области связывания. Каждый ион окружен сферическим электрическим полем, действующим на любой другой ион вне зависимости от места его расположения. [2]
Ионная химическая связь представляет собой электростатическое взаимодействие отрицательно и положительно заряженных ионов в химическом соединении. [3]
Ионной химической связью называют связь, которая образуется I между катионом и анионом в результате их электростатического - взаимодействия. [4]
Отсутствие у ионной химической связи такого свойства, как насыщаемость и направленность, приводит к образованию ионных кристаллов, представляющих собой, по существу, гигантские полимерные молекулы. Каждый ионный кристалл, как гигантская молекула, может и дальше увеличиваться в размерах путем присоединения к поверхности кристалла в процессе кристаллизации новых положительных и отрицательных ионов. [5]
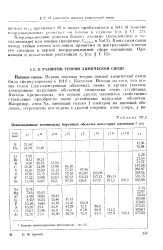 |
Ионизационные потенциалы наружных оболочек некоторых элементов ( эв. [6] |
Первая научная теория ионной химической связи была сформулирована в 1916 г. Косселем. Исходя из того, что атомы гелия ( двухэлектронная оболочка), неона и аргона ( восьмп-электронные наружные оболочки) химически очень устойчивы, Коссель предположил, что атомам других элементов свойственно стремление приобрести такие устойчивые наружные оболочки. [7]
Первая научная теория ионной химической связи была сформулирована в 1916 г. Косселем. Исходя из того, что атомы гелия ( двухэлектронная наружная оболочка), неона и аргона ( вось-миэлектронные наружные оболочки) химически очень устойчивы, Коссель предположил, что атомам других элементов свойственно стремление приобрести такие устойчивые наружные оболочки. Например, атом Na, имеющий только один электрон на внешней оболочке, стремится его отдать; с другой стороны, атом хлора, у которого не хватает одного электрона до внешней оболочки аргона, стремится его приобрести. [8]
Представителями группы веществ с ионной химической связью являются щелочно-галогенистые соединения. [9]
К твердым веществам с ионной химической связью, к бесконечным трехмерным кристаллам законы постоянства состава и простых кратных отношений неприменимы. Любой, даже чистый стехиометрический кристалл выше О К всегда станет нестехио-метрическим из-за теплового движения атомов или ионов, часть которых может покинуть поверхность вещества. Кроме того, любой идеальный кристалл стехиометрического соединения АлВт не отвечает закону постоянства состава, так как он может содержать переменное число молекул ( АпВт) л в зависимости от своего размера. [10]
Томсон нарисовал следующую картину образования ионной химической связи. При соединении атомов электроположительных и электроотрицательных элементов, в результате того, что в первых электроны ( корпускулы, по терминологии Томсона) удерживаются относительно слабо, а во-вторых - очень прочно, возможно отделение электронов от электроположительных атомов и переход к электроотрицательным. Электроотрицательные атомы получают, таким образом, заряд отрицательного электричества, электроположительные атомы - заряд положительного электричества, противоположно заряженные атомы будут притягиваться друг к другу, и образуется химическое соединение электроположительных и электроотрицательных атомов [ 75, с. В том же, 1904 г. Томсон развил взгляд на химическую связь, как на единичную фарадеевскую трубку, связывающую заряженные атомы в молекуле. [11]
Томсон нарисовал следующую картину образования ионной химической связи. При соединении атомов электроположительных и электроотрицательных элементов, в результате того, что в первых электроны ( корпускулы, по терминологии Томсона) удерживаются относительно слабо, а во-вторых - очень прочно, возможно отделение электронов от электроположительных атомов и переход к электроотрицательным. Электроотрицательные атоцы получают, таким образом, заряд отрицательного электричества, электроположительные атомы - заряд положительного электричества, противоположно заряженные атомы будут притягиваться друг к другу, и образуется химическое соединение электроположительных и электроотрицательных атомов [ 75, с. В том же, 1904 г. Томсон развил взгляд на химическую связь, как на единичную фарадеевскую трубку, связывающую заряженные атомы в молекуле. [12]
Различное поведение электронов и дырок в кристаллах с ковалентной и ионной химической связью обусловлено различным характером взаимодействия избыточного электрона с окружающей средой кристалла. В любом веществе избыточный электрон, находящийся в зоне проводимости, или дырка в валентной зоне поляризуют окружающую среду. В телах, состоящих из нейтральных атомов, таких, как валентные полупроводники, поляризация сводится к образованию электрических диполей на каждом из окружающих атомов благодаря смещению их внешних электронных оболочек относительно положительного ионного остатка. Такой вид поляризации соответствует высокочастотной ( оптической) диэлектрической постоянной и характеризуется очень малым временем релаксации, при котором поляризационное искажение среды успевает следовать за вызвавшим его избыточным электроном при движении последнего по кристаллу. [13]
 |
Перекрывание электронных облаков при образовании молекулы. [14] |
Так как электрическое поле иона имеет сферический характер, то для ионной химической связи не характерна направленность. Ионной связи также не свойственна насыщаемость, так как ион способен взаимодействовать со многими соседними ионами противоположного знака, число которых зависит от зарядов ионов и соотношений геометрических размеров. Ионная химическая связь проявляется в твердых веществах с ионной кристаллической решеткой, свойства которых будут рассмотрены в гл. Так как энергия ионизации больше энергии сродства к электрону, то полного перехода электронов не происходит даже в случае пары атомов с большой разностью ЭО. Поэтому и чисто ионная связь не существует. [15]
Страницы: 1 2 3 4