Ионная химическая связь
Cтраница 2
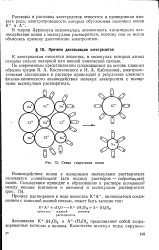 |
Схема гидратации ионов. [16] |
К электролитам относятся вещества, в молекулах которых атомы связаны сильно полярной или ионной химической связью. [17]
Ионные кристаллы образованы противоположно заряженными ионами ( простыми или сложными), объединяемыми вместе ионной химической связью. Ионы не являются, как правило, сферическими и в зависимости от числа окружающих их противоионов могут сжиматься и расширяться. Так как чисто электростатическое взаимодействие ионов не имеет направленности, каждый ион стремится окружить себя как можно большим числом ионов противоположного знака. Поэтому в ионных кристаллах нельзя выделить дискретные обособленные молекулы, каждый ионный кристалл следует рассматривать как одну гигантскую молекулу. Ионные кристаллы отличают большая твердость, высокие температуры плавления, малая летучесть, слабая деформируемость, а следовательно, высокая хрупкость. [18]
Соединение катиона большой поляризующей силы с легко поляризующимся анионом приводит к образованию уже не чисто ионной химической связи, а ковалентной или гомеополярной. [19]
Соединение катиона большой поляризующей силы с легко поляризующимся анионом приводит к образованию уже не чисто ионной химической связи, а ковалентнон или гомеополярной. [20]
Соединение катиона большой поляризующей силы с легко поляризующимся анионом приводит к образованию уже не чисто ионной химической связи, а ковалентной или гомеополярной. [21]
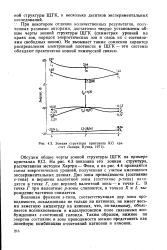 |
Зонная структура кристалла КС1 ( расчет Линари, Кунца, 1971. [22] |
Не вызывает также сомнения характер распределения электронной плотности в ЩГК - эти системы обладают практически ионной химической связью. [23]
 |
Схема и модель кристаллической решетки хлорида натрия. [24] |
Молекулы, образованные из противоположно заряженных ионов, называют ионными молекулами, а химическая связь, в таких молекулах - ионной химической связью. Ионные молекулы характерны для соединений, образовавшихся из атомоз щелочных металлов и галогенов. [25]
Кремний, кислород, алюминий и множество тяжелых поливалентных элементов образуют природные линейные и трехмерные полимеры - минералы, построенные посредством высокополяризованных и ионных химических связей. В то же время элементы органогены - углерод, водород, кислород, азот, расположенные в I и II периодах таблицы Д. И. Менделеева, для которых характерны относительно малополярньте химические связи, служат основой огромного большинства как до сих пор полученных в лабораториях, так и выпускаемых промышленностью синтетических полимеров. Такие чисто органические полимеры, в отличие от минеральных, обладают оптимальным сочетанием относительной стабильности и изменчивости, способностью проявлять весьма разные свойства в зависимости от состава, строения, способов модификации и переработки. [26]
Чем дальше отстоят друг от друга элементы на диаграмме, тем больше разность их электроотрицательностей и тем ближе связь между ними к ионной химической связи. Al, Mg, Ti и др., достаточно велика для того, чтобы связь между ними можно было рассматривать практически как ионную. Этот вывод справедлив также и для окислив переходных металлов Mn, Fe, Co, Ni и др., которые не приведены на фиг. [27]
Физическое обоснование идея Абегга и Бодлендера приобрела впервые у Томсона ( 1904 г.), который на основе своей теории строения атома дал модельное представление об электроотрицательных и электроположительных элементах, их расположении в периодической системе, а также о соединении электроотрицательных и электроположительных элементов с образованием ионной химической связи [ 19, стр. [28]
Соли s - элементов известны практически для всех кислот. Обычно это бесцветные кристаллические вещества с ионной химической связью ( кроме ряда соединений бериллия), обладающие высокими температурами плавления, электрической проводимостью своих растворов в воде и расплавов. [29]
При контакте двух тел, весьма различных по своей химической природе, существенная часть контактной разности потенциалов распределяется в очень тонком пограничном слое, толщина которого равна расстоянию между атомами в соприкасающихся телах. Такое распределение контактной разности потенциала соответствует образованию полярных или ионных химических связей между поверхностными атомами рассматриваемых тел. Остальная часть контактной разности потенциалов распределяется в слоях пространственного заряда соприкасающихся тел. [30]
Страницы: 1 2 3 4